Klorreaktivitet:Forståelse af kemiske reaktioner og forbindelser
* Høj elektronegativitet: Klor har en høj elektronegativitet, hvilket betyder, at det stærkt tiltrækker elektroner. Dette gør den ivrig efter at få en elektron for at opnå en stabil elektronkonfiguration.
* Syv valenselektroner: Klor har syv elektroner i sin yderste skal. Den behøver kun en elektron mere for at opnå en hel oktet, hvilket gør den meget reaktiv.
Eksempler på klorreaktioner:
* Metaller: Klor reagerer let med de fleste metaller og danner metalchlorider. For eksempel reagerer natrium voldsomt med klorgas og danner natriumchlorid (NaCl), som er almindeligt bordsalt.
* Ikke-metaller: Klor reagerer også med mange ikke-metaller. For eksempel reagerer det med brint og danner hydrogenchlorid (HCl), en stærk syre.
* Økologiske forbindelser: Klor reagerer med organiske forbindelser og danner chlorerede forbindelser. Dette bruges til fremstilling af plastik, pesticider og lægemidler.
Bemærk: Klorreaktioner kan være meget eksoterme, hvilket betyder, at de frigiver meget varme. Nogle reaktioner kan være eksplosive eller farlige. Det er vigtigt at håndtere klor med forsigtighed.
Sidste artikelKobbersulfat og sandadskillelse:En trin-for-trin guide
Næste artikelStøkiometri af MgCl2 og KOH Reaktion:Moles &Ratio
 Varme artikler
Varme artikler
-
 Forskere udvikler solid-state, fritstående carbon nanofiber superkondensatorDrexel-forskere har udviklet en solid-state, fritstående elektrode, der kan gøre energilagringsenheder sikrere ved at fjerne deres brændbare elektrolytopløsning. Elektroden bruger en kulfibermåtte, la
Forskere udvikler solid-state, fritstående carbon nanofiber superkondensatorDrexel-forskere har udviklet en solid-state, fritstående elektrode, der kan gøre energilagringsenheder sikrere ved at fjerne deres brændbare elektrolytopløsning. Elektroden bruger en kulfibermåtte, la -
 Forskere klemmer katalysatorer inde i værtsmaterialer som et skib i en flaskeVed hjælp af termodynamiske Pourbaix-diagrammer, videnskabsmænd kan presse katalysatorer inde i værtsmaterialer som et skib i en flaske. Kredit:Jingwei Hou Forskere ved Queen Mary University of Lo
Forskere klemmer katalysatorer inde i værtsmaterialer som et skib i en flaskeVed hjælp af termodynamiske Pourbaix-diagrammer, videnskabsmænd kan presse katalysatorer inde i værtsmaterialer som et skib i en flaske. Kredit:Jingwei Hou Forskere ved Queen Mary University of Lo -
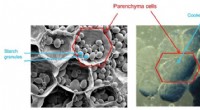 Ny forarbejdningsteknik kan gøre kartofler sundereMikroskopisk billede af kartoffelvæv før (venstre) og efter (højre) kogning eller forarbejdning. Kredit:Amy Lin, A*STAR, og Yijing Shao og YuLian Lin, University of Idaho. Forskere annoncerede tidl
Ny forarbejdningsteknik kan gøre kartofler sundereMikroskopisk billede af kartoffelvæv før (venstre) og efter (højre) kogning eller forarbejdning. Kredit:Amy Lin, A*STAR, og Yijing Shao og YuLian Lin, University of Idaho. Forskere annoncerede tidl -
 Kemikere udnytter lysets kraft til at tackle asymmetriske molekylerFSU-forskere brugte lys til at forvandle et venstrehåndsmolekyle til et højrehåndet. Kredit:Adjunkt i kemi Ken Hanson Ingen, molekyler har faktisk ikke hænder. Men videnskabsmænd omtaler dem på de
Kemikere udnytter lysets kraft til at tackle asymmetriske molekylerFSU-forskere brugte lys til at forvandle et venstrehåndsmolekyle til et højrehåndet. Kredit:Adjunkt i kemi Ken Hanson Ingen, molekyler har faktisk ikke hænder. Men videnskabsmænd omtaler dem på de
- Ionisk eller kovalent? Forstå bindingen i jernsulfid (FeS)
- Hvordan påvirker tyngdekraften lagene på jorden?
- Hvordan er tyngdekraften mellem genstande, der har små masser sammenlignet med store genstande?
- Hvad er bevaret i Gene Bank?
- NASAs Aqua-satellit finder en tropisk cyklon-sandwich
- Hvordan flyder elektroner i katodisk beskyttelse?


