Molekylære forbindelser og elektrisk ledningsevne:En omfattende forklaring
* Mangel på gratis operatører: Molekylære forbindelser dannes ved deling af elektroner mellem atomer for at danne kovalente bindinger. Disse elektroner holdes tæt inde i molekylet og er ikke frie til at bevæge sig gennem hele materialet. Det betyder, at der er meget få, hvis nogen, gratis ladningsbærere til at bære en elektrisk strøm.
* Ingen ioner: I modsætning til ioniske forbindelser, som har ladede ioner, der kan bevæge sig frit, har molekylære forbindelser ikke frie ioner. Dette begrænser yderligere deres evne til at lede elektricitet.
Undtagelser:
Mens de fleste molekylære forbindelser er dårlige ledere, er der nogle undtagelser:
* Smeltede eller vandige opløsninger: Nogle molekylære forbindelser, som vand med opløste syrer eller baser, kan lede elektricitet, når de er i flydende tilstand. Det skyldes, at de opløste molekyler kan dissociere til ioner, som så kan føre en strøm.
* Grafit: Grafit er en form for kulstof med en unik struktur, der giver mulighed for bevægelse af elektroner i dets lag. Dette gør grafit til en god leder af elektricitet.
Opsummering:
Molekylære forbindelser er generelt dårlige ledere af elektricitet, fordi de mangler frie ladningsbærere og ioner. Der findes dog nogle undtagelser, især i tilfælde, hvor molekylerne kan dissociere til ioner eller have en unik struktur, der giver mulighed for elektronbevægelse.
Sidste artikelFedtsyrer vs. Glycerol:Forståelse af lipidbyggesten
Næste artikelSaltsyre vs. hydrogenchlorid:Vigtigste forskelle forklaret
 Varme artikler
Varme artikler
-
 Molekylær lokkemad kan hjælpe hydrogeler med at hele sårHydrogeler udviklet ved Rice University inkorporerer tværbindere, der kan inkorporere bioaktive molekyler og hjælpe med at hele en række forskellige sår. Kredit:Jeff Fitlow/Rice University Ligesom
Molekylær lokkemad kan hjælpe hydrogeler med at hele sårHydrogeler udviklet ved Rice University inkorporerer tværbindere, der kan inkorporere bioaktive molekyler og hjælpe med at hele en række forskellige sår. Kredit:Jeff Fitlow/Rice University Ligesom -
 Origami-diagnostisk enhed tilbyder overkommelige malariadiagnoserPapirfoldningstrin til fluidisk manipulation. Skema over, hvordan papirstrimlen i den mikrofluidiske enhed foldes for hvert trin. Pilene angiver foldningsretningen. Kredit:Niall P. Macdonald (Dublin C
Origami-diagnostisk enhed tilbyder overkommelige malariadiagnoserPapirfoldningstrin til fluidisk manipulation. Skema over, hvordan papirstrimlen i den mikrofluidiske enhed foldes for hvert trin. Pilene angiver foldningsretningen. Kredit:Niall P. Macdonald (Dublin C -
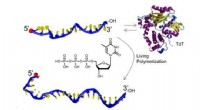 Oddball-enzym giver nem vej til syntetiske biomaterialerNy opskrift bruger overset DNA-builder til at forenkle produktionen af syntetiske biomaterialer til applikationer lige fra lægemiddellevering til nanotråde. Kredit:Stefan Zauscher, Duke University
Oddball-enzym giver nem vej til syntetiske biomaterialerNy opskrift bruger overset DNA-builder til at forenkle produktionen af syntetiske biomaterialer til applikationer lige fra lægemiddellevering til nanotråde. Kredit:Stefan Zauscher, Duke University -
 En mere sikker måde at fremstille azider til brug i klikkemien, Syntese af FSO2N3. Reaktionsbetingelser:1 (7,9 g, 24 mmol), NaN3 (1,3 g, 20 mmol), MTBE/MeCN/H2O (84 ml, 10:1:10, v/v/v), 0 °C, luft, 10 min. b, Diazotransferreaktion mellem amlodipin (2a) og FSO2
En mere sikker måde at fremstille azider til brug i klikkemien, Syntese af FSO2N3. Reaktionsbetingelser:1 (7,9 g, 24 mmol), NaN3 (1,3 g, 20 mmol), MTBE/MeCN/H2O (84 ml, 10:1:10, v/v/v), 0 °C, luft, 10 min. b, Diazotransferreaktion mellem amlodipin (2a) og FSO2
- Hvor mange mol iod produceres fra 8,00 klor?
- Hvilken bjergkæde dannede sig, da pladen indeholdende indisk subkontinent bombede til kontinentet i…
- Vitamin B12:Bioinorganisk kemi, struktur og nøglereaktioner
- Facebook-chef står over for Europa-Parlamentet over dataskandale
- Hvor mange valenselektroner skal rummes i Lewis-strukturen for LiCl?
- 3D-simulering viser, hvordan form af komplekse organer udvikler sig ved naturlig udvælgelse


