Ioniske forbindelser:Dannelse, elementer og eksempler | Kemi forklaret
Her er en opdeling:
* Metaller har tendens til at miste elektroner og danne kationer .
* Ikke-metaller har tendens til at få elektroner og danne anioner .
Nøgleelementer, der danner ioniske forbindelser:
* Metaller: Gruppe 1 (alkalimetaller), 2 (jordalkalimetaller), 3 (overgangsmetaller) og nogle grundstoffer fra gruppe 13, 14 og 15.
* Ikke-metaller: Gruppe 16 (chalcogener) og 17 (halogener).
Eksempler:
* Natriumchlorid (NaCl) :Natrium (Na) er et metal i gruppe 1, og klor (Cl) er et ikke-metal i gruppe 17. Natrium mister en elektron for at blive en kation (Na+), mens klor får en elektron til at blive en anion (Cl-). Disse modsat ladede ioner tiltrækker og danner den ioniske forbindelse NaCl.
* Magnesiumoxid (MgO) :Magnesium (Mg) er et metal i gruppe 2, og oxygen (O) er et ikke-metal i gruppe 16. Magnesium mister to elektroner for at blive en kation (Mg2+), mens oxygen får to elektroner til at blive en anion (O2-). Disse ioner tiltrækker for at danne MgO.
Undtagelser:
* Ammoniumion (NH4+) er en polyatomisk kation dannet af kombinationen af nitrogen og hydrogen.
* Hydroxidion (OH-) er en polyatomisk anion dannet af kombinationen af oxygen og hydrogen.
Opsummering:
Ioniske forbindelser dannes af kombinationen af elementer, der let taber eller vinder elektroner, hvilket resulterer i dannelsen af positivt og negativt ladede ioner, der tiltrækker hinanden på grund af elektrostatiske kræfter.
 Varme artikler
Varme artikler
-
 Kemikere opdager, hvordan blåt lys fremskynder blindhedDr. Ajith Karunarathne undersøgte giftig iltgenerering af retinal under eksponering for blåt lys. Kredit:Dan Miller, Universitetet i Toledo Blåt lys fra digitale enheder og solen forvandler vitale
Kemikere opdager, hvordan blåt lys fremskynder blindhedDr. Ajith Karunarathne undersøgte giftig iltgenerering af retinal under eksponering for blåt lys. Kredit:Dan Miller, Universitetet i Toledo Blåt lys fra digitale enheder og solen forvandler vitale -
 Forskere udvikler syntetiske T -celler, der efterligner form, funktion af menneskelig versionUCLA -forskere udviklede kunstige T -celler, der, som naturlige T -celler, kan deformere for at klemme mellem små huller i kroppen, som vist i denne skema. Kredit:Fatemeh Majedi UCLA -forskere har
Forskere udvikler syntetiske T -celler, der efterligner form, funktion af menneskelig versionUCLA -forskere udviklede kunstige T -celler, der, som naturlige T -celler, kan deformere for at klemme mellem små huller i kroppen, som vist i denne skema. Kredit:Fatemeh Majedi UCLA -forskere har -
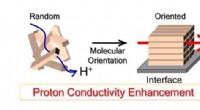 Få mere kontrol over brændselscellemembranerMolekylær orientering forbedrer protonkonduktion i protonkonduktive polymerer. Kredit:Yuki Nagao Mere organisering på molekylært niveau kan forbedre effektiviteten af membraner, der bruges i bri
Få mere kontrol over brændselscellemembranerMolekylær orientering forbedrer protonkonduktion i protonkonduktive polymerer. Kredit:Yuki Nagao Mere organisering på molekylært niveau kan forbedre effektiviteten af membraner, der bruges i bri -
 Kunstig intelligens hjælper forskere med at producere rekordsættende katalysator til kuldioxid-til…Forskere fra U of T Engineering og Carnegie Mellon University bruger elektrolysatorer som denne til at omdanne affalds-CO2 til kommercielt værdifulde kemikalier. Deres seneste katalysator, designet ti
Kunstig intelligens hjælper forskere med at producere rekordsættende katalysator til kuldioxid-til…Forskere fra U of T Engineering og Carnegie Mellon University bruger elektrolysatorer som denne til at omdanne affalds-CO2 til kommercielt værdifulde kemikalier. Deres seneste katalysator, designet ti
- Forskere udvikler grønnere plast - den større udfordring er at flytte dem fra laboratorium til mar…
- Geologer bliver kaldt beskidte forurenere, men var nødvendige for at bekæmpe klimaændringer
- Calciummetal- og salpetersyrereaktion:Produkter, forklaring og sikkerhed
- Hvordan udforsker du hydrotermiske ventilationsåbninger?
- Hvorfor og hvornår fandt rumkapløbet sted?
- Næsten 60 % af iværksætterne i Indien rapporterer positiv indvirkning af COVID-19 på deres virks…


