Dobbelt kovalent binding mellem iltatomer:forklaring og dannelse
* Oxygens elektroniske konfiguration: Ilt har seks elektroner i sin ydre skal (valensskal). Den har brug for to elektroner mere for at opnå en stabil oktet (otte elektroner).
* Deling af elektroner: For at opnå denne stabilitet deler to oxygenatomer to par elektroner og danner en dobbelt kovalent binding. Denne deling tillader hvert iltatom at have otte elektroner i sin ydre skal.
Repræsentation:
Den dobbelte kovalente binding mellem to oxygenatomer er ofte repræsenteret ved følgende:
O=O
Denne notation viser, at to par elektroner deles mellem de to oxygenatomer.
Sidste artikelLavt smeltepunktsbindinger:Forstå Van der Waals &Hydrogen Bonds
Næste artikelVands polaritet:unikke egenskaber og betydning
 Varme artikler
Varme artikler
-
 Kemiker får en nanokatalysatorbase fra risskallerEn kemiker fra RUDN udviklede en metode til at opnå siliciumdioxid med høj porøsitet fra risskaller. Kredit:Allen Dressen En kemiker fra RUDN har udviklet en metode til opnåelse af siliciumdioxid
Kemiker får en nanokatalysatorbase fra risskallerEn kemiker fra RUDN udviklede en metode til at opnå siliciumdioxid med høj porøsitet fra risskaller. Kredit:Allen Dressen En kemiker fra RUDN har udviklet en metode til opnåelse af siliciumdioxid -
 Små oplyste stregkoder identificerer molekyler ved deres blinkDisse små lyspunkter kan ligne stjerner, der blinker på himlen. Men i virkeligheden er de forskellige molekyler af oplyst DNA, blinker til og fra, mens de binder og afbinder under et mikroskop. Kredit
Små oplyste stregkoder identificerer molekyler ved deres blinkDisse små lyspunkter kan ligne stjerner, der blinker på himlen. Men i virkeligheden er de forskellige molekyler af oplyst DNA, blinker til og fra, mens de binder og afbinder under et mikroskop. Kredit -
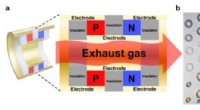 En termoelektrisk blæk, der gør bilens udstødningsrør til kraftgeneratorer3D-print af kraftproducerende TE-rør. a) Skema, der viser det kraftgenererende TE-rør fremstillet af 3D-printede p-type og n-type PbTe-rør forfra. b) Foto, der viser komponenterne til modulets samling
En termoelektrisk blæk, der gør bilens udstødningsrør til kraftgeneratorer3D-print af kraftproducerende TE-rør. a) Skema, der viser det kraftgenererende TE-rør fremstillet af 3D-printede p-type og n-type PbTe-rør forfra. b) Foto, der viser komponenterne til modulets samling -
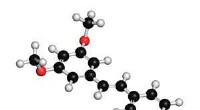 Palladiumkatalysator fremskynder to separate reaktioner, fremstilling af nyttige molekyler i en enke…Pterostilbene (billedet), et defensivt kemikalie fundet i blåbær, er et eksempel på et funktionelt molekyle, der indeholder stilben-motivet. Kredit:MOLEKUUL/SCIENCE PHOTO LIBRARY En palladiumkatal
Palladiumkatalysator fremskynder to separate reaktioner, fremstilling af nyttige molekyler i en enke…Pterostilbene (billedet), et defensivt kemikalie fundet i blåbær, er et eksempel på et funktionelt molekyle, der indeholder stilben-motivet. Kredit:MOLEKUUL/SCIENCE PHOTO LIBRARY En palladiumkatal
- Hvilke værktøjer brugte Neil Armstrong til at studere måneoverfladen?
- Essay:Vil den første ændring overleve informationsalderen?
- Hvor foregår aktiv havbundspredning i dag?
- Udvikler til at åbne hub til vækst i amerikansk havvindindustri
- Hvilken klippe den smelter under Jorden?
- Mulige beviser for limkugler fundet under Beijing Spectrometer III eksperimenter


