Lavt smeltepunktsbindinger:Forstå Van der Waals &Hydrogen Bonds
* Van der Waals styrker: Disse er de svageste intermolekylære kræfter og er ansvarlige for smeltepunkterne for ikke-polære molekyler som metan (CH4). De overvindes let af termisk energi, hvilket resulterer i lave smeltepunkter.
* Brintbindinger: Selvom de er stærkere end Van der Waals-kræfterne, er hydrogenbindinger stadig relativt svage sammenlignet med kovalente eller ioniske bindinger. De spiller en væsentlig rolle i smeltepunkterne for stoffer som vand, der smelter ved 0°C.
* ioniske bindinger: Disse er stærkere end hydrogenbindinger, men svagere end kovalente bindinger. Ioniske forbindelser har ofte moderate smeltepunkter, afhængigt af størrelsen og ladningen af de involverede ioner. For eksempel smelter natriumchlorid (NaCl) ved 801°C.
* Kovalente bindinger: Disse er den stærkeste type kemisk binding. Forbindelser holdt sammen af kovalente bindinger har typisk høje smeltepunkter. For eksempel smelter diamant, et netværk af kovalent bundne carbonatomer, ved 3550°C.
Her er nogle yderligere faktorer, der påvirker smeltepunktet:
* Molekylvægt: Større molekyler har en tendens til at have højere smeltepunkter på grund af øgede Van der Waals-kræfter.
* Symmetri: Symmetriske molekyler pakker mere effektivt, hvilket fører til stærkere intermolekylære kræfter og højere smeltepunkter.
* Polaritet: Polære molekyler har højere smeltepunkter end ikke-polære molekyler på grund af dipol-dipol-interaktioner.
Opsummering: Styrken af de bindinger, der holder et stof sammen, er den primære faktor, der bestemmer dets smeltepunkt. Svagere bindinger, såsom Van der Waals-kræfter og hydrogenbindinger, resulterer i lavere smeltepunkter, mens stærkere bindinger som kovalente bindinger fører til højere smeltepunkter.
 Varme artikler
Varme artikler
-
 Biokemiske netværk kortlagt i mellemtarmen af Aedes aegypti-mygAdjunkt Rushika Perera og kandidatstuderende Rebekah Gullberg på arbejde på Laboratoriet for leddyrbårne og infektionssygdomme. Kredit:William A. Cotton/Colorado State University Photography I løb
Biokemiske netværk kortlagt i mellemtarmen af Aedes aegypti-mygAdjunkt Rushika Perera og kandidatstuderende Rebekah Gullberg på arbejde på Laboratoriet for leddyrbårne og infektionssygdomme. Kredit:William A. Cotton/Colorado State University Photography I løb -
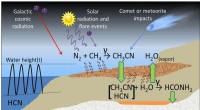 Opstod vandbaseret liv uden vand?Foreslået proces til formamidsyntese nær radioaktive mineralaflejringer på Jordens overflade. Kredit:Adam et al. Udgivet i Videnskabelige rapporter . Når man forsøger at forstå oprindelsen af
Opstod vandbaseret liv uden vand?Foreslået proces til formamidsyntese nær radioaktive mineralaflejringer på Jordens overflade. Kredit:Adam et al. Udgivet i Videnskabelige rapporter . Når man forsøger at forstå oprindelsen af -
 4140 Stål:hærdning, bearbejdning og praktiske anvendelserAf Tony Oldhand | Opdateret 24. marts 2022 Hærdende egenskaber Når 4140 stål kommer ud af ovnen, er det et blødt metal. Opvarmning af det til næsten smeltning og derefter hurtig afkøling - typisk ved
4140 Stål:hærdning, bearbejdning og praktiske anvendelserAf Tony Oldhand | Opdateret 24. marts 2022 Hærdende egenskaber Når 4140 stål kommer ud af ovnen, er det et blødt metal. Opvarmning af det til næsten smeltning og derefter hurtig afkøling - typisk ved -
 Tredimensionelt billede af katalysatorer i aktionOperando røntgenspektroskopi viser, hvad der sker i hver enkelt del af en fungerende katalysator. Kredit:Dr. Dmitry Doronkin, KIT For at forstå strukturen og funktionen af katalysatorer i aktion
Tredimensionelt billede af katalysatorer i aktionOperando røntgenspektroskopi viser, hvad der sker i hver enkelt del af en fungerende katalysator. Kredit:Dr. Dmitry Doronkin, KIT For at forstå strukturen og funktionen af katalysatorer i aktion
- Biologer bruger den videnskabelige metode til at svare på?
- Jo tungere en genstand er den større kraft, der er nødvendig for at flytte den?
- En ny vej til cancerterapi:Udvikling af simultan multiplekset genredigeringsteknologi
- Høje niveauer af PFAS påvirker immunforsvaret, leverfunktioner i Cape Fear River stribet bas
- Hvad er dycenteri?
- Glimt af håb, mens Italien kæmper mod spedalskhed fra oliventræer


