Van der Waals ligning:Faktorer, der forårsager reelle gasafvigelser
1. Intermolekylære kræfter: Ideelle gasser antages ikke at have nogen interaktion mellem deres molekyler. Men ægte gasser udviser svage tiltrækningskræfter, kendt som van der Waals-kræfter. Disse kræfter opstår fra midlertidige fluktuationer i elektronfordelingen omkring molekyler, hvilket fører til midlertidige dipoler, der tiltrækker nabomolekyler. Denne tiltrækning reducerer trykket, som gassen udøver, sammenlignet med, hvad man ville forvente af den ideelle gaslov.
2. Endelig volumen af gasmolekyler: Ideelle gasser antages at have nul volumen. I virkeligheden optager molekyler et begrænset volumen. Det betyder, at den ledige plads, der er til rådighed for molekylerne at bevæge sig rundt i, er mindre end beholderens samlede volumen. Denne reduktion i tilgængeligt volumen øger trykket, der udøves af gassen, sammenlignet med, hvad man ville forvente af den ideelle gaslov.
Disse to faktorer, intermolekylære kræfter og endeligt molekylært volumen, er redegjort for i van der Waals-ligningen, som giver en mere præcis beskrivelse af reel gasadfærd end den ideelle gaslov.
 Varme artikler
Varme artikler
-
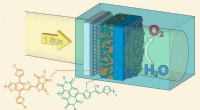 Et kunstigt blad lavet af halvledende polymererGenerering af ilt fra sollys, vand og halvledende polymerer. Kredit:LIMNO / EPFL EPFL-forskere genererer ilt fra sollys, vand og halvledende polymerer. De præsenterer en lovende vej mod økonomisk
Et kunstigt blad lavet af halvledende polymererGenerering af ilt fra sollys, vand og halvledende polymerer. Kredit:LIMNO / EPFL EPFL-forskere genererer ilt fra sollys, vand og halvledende polymerer. De præsenterer en lovende vej mod økonomisk -
 Klistermærker og en smartphone til nem nitritpåvisning på fødevarerEn ny film reagerer på nitritanioner gennem en farveændring, der bliver mørkere med højere nitritniveauer. Kredit:Tilpasset fra ACS Applied Materials &Interfaces 2022, DOI:10.1021/acsami.2c09467 Ni
Klistermærker og en smartphone til nem nitritpåvisning på fødevarerEn ny film reagerer på nitritanioner gennem en farveændring, der bliver mørkere med højere nitritniveauer. Kredit:Tilpasset fra ACS Applied Materials &Interfaces 2022, DOI:10.1021/acsami.2c09467 Ni -
 Forståelse af latent varmeoverførsel:nøglebegreber og energilagringsapplikationerAf Chris Rowe Opdateret 24. marts 2022 Overgangen mellem et materiales faste, flydende og gasformige faser involverer store mængder energi. Dette energibehov er kendt som latent varmeoverførsel. For
Forståelse af latent varmeoverførsel:nøglebegreber og energilagringsapplikationerAf Chris Rowe Opdateret 24. marts 2022 Overgangen mellem et materiales faste, flydende og gasformige faser involverer store mængder energi. Dette energibehov er kendt som latent varmeoverførsel. For -
 Videnskabelige fremskridt kan gøre det lettere at genanvende plastKredit:CC0 Public Domain De fleste af de 150 millioner tons plastik, der produceres rundt om i verden hvert år, ender på lossepladser, havene og andre steder. Mindre end 9 procent af plasten genan
Videnskabelige fremskridt kan gøre det lettere at genanvende plastKredit:CC0 Public Domain De fleste af de 150 millioner tons plastik, der produceres rundt om i verden hvert år, ender på lossepladser, havene og andre steder. Mindre end 9 procent af plasten genan


