Kemisk ligevægt:Reaktant vs. produktmængder
Her er hvorfor:
* Ligevægt er en dynamisk tilstand: Det er ikke en statisk situation, hvor reaktionen er stoppet. I stedet for sker de fremadrettede og omvendte reaktioner med samme hastighed . Dette betyder, at hastigheden af dannelsen af produkter er lig med hastigheden af dannelsen af reaktanter.
* Relative beløb: Mens *hastighederne* er ens, kan *mængderne* af reaktanter og produkter være meget forskellige. De relative mængder afhænger af ligevægtskonstanten (K).
* K> 1: Foretrækker produkter. Der vil være flere produkter end reaktanter ved ligevægt.
* K <1: Begunstiger reaktanter. Der vil være flere reaktanter end produkter ved ligevægt.
* K =1: Ligevægt opnås, når mængderne af reaktanter og produkter er lige store.
Eksempel: Tænk på en reversibel reaktion, hvor A + B <-> C + D. Ved ligevægt er reaktionen ikke stoppet; det er bare, at dannelseshastigheden for C og D er lig med dannelseshastigheden for A og B. Der kan være meget mere C og D til stede, eller meget mere A og B, afhængigt af værdien af K.
 Varme artikler
Varme artikler
-
 Blæksprutteskind inspirerer til skabelsen af næste generations rumtæppeAlon Gorodetsky, UCI lektor i kemisk og biomolekylær teknik, og Erica Leung, en UCI kandidatstuderende i den afdeling, har opfundet et nyt materiale, der kan fange eller frigive varme efter ønske. Kre
Blæksprutteskind inspirerer til skabelsen af næste generations rumtæppeAlon Gorodetsky, UCI lektor i kemisk og biomolekylær teknik, og Erica Leung, en UCI kandidatstuderende i den afdeling, har opfundet et nyt materiale, der kan fange eller frigive varme efter ønske. Kre -
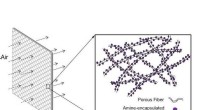 En bedre kulstoffælde vil tage drivhusgasser ud af luften og tage dem i brugKredit:Rensselaer Polytekniske Institut Kulstoffangstteknologier spiller en afgørende rolle i at reducere drivhusgasemissioner fra kraftværker og fabrikker, mens du udnytter kuldioxid (CO 2 ) ti
En bedre kulstoffælde vil tage drivhusgasser ud af luften og tage dem i brugKredit:Rensselaer Polytekniske Institut Kulstoffangstteknologier spiller en afgørende rolle i at reducere drivhusgasemissioner fra kraftværker og fabrikker, mens du udnytter kuldioxid (CO 2 ) ti -
 Høj opløsning, terahertz-drevet atomprobe tomografiIonfeltfordampning udløst af terahertz i en tomografisk atomprobe. (A) Ultrashort terahertz (røde) pulser er fokuseret på en metallisk nanotip inde i et højvakuumkammer. Den højspænding, der påføres d
Høj opløsning, terahertz-drevet atomprobe tomografiIonfeltfordampning udløst af terahertz i en tomografisk atomprobe. (A) Ultrashort terahertz (røde) pulser er fokuseret på en metallisk nanotip inde i et højvakuumkammer. Den højspænding, der påføres d -
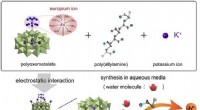 Hybridmateriale flytter næste generations transportbrændstofceller tættere påUltrahøj protonkonduktion i polyoxometalatbaseret ramme Billedtekst:Ultrahøj protonkonduktion via udvidet hydrogenbindingsnetværk i polyoxometalatbaseret ramme, der er funktionaliseret med Lanthanide
Hybridmateriale flytter næste generations transportbrændstofceller tættere påUltrahøj protonkonduktion i polyoxometalatbaseret ramme Billedtekst:Ultrahøj protonkonduktion via udvidet hydrogenbindingsnetværk i polyoxometalatbaseret ramme, der er funktionaliseret med Lanthanide


