Dannelse af jernsulfid (FeS):Kemiske reaktioner og processer
1. Direkte reaktion af jern og svovl:
* Høje temperaturer: Når jern og svovl opvarmes sammen ved høje temperaturer, reagerer de direkte og danner jernsulfid. Reaktionen er meget eksoterm:
```
Fe(s) + S(s) → FeS(s)
```
2. Reaktioner i vandige opløsninger:
* Reaktion af jernsalte med sulfider: I opløsninger, der indeholder jern(II)-ioner (Fe²⁺) og sulfidioner (S²⁻), udfældes jern(II)-sulfid som et sort fast stof:
```
Fe²⁺(aq) + S²⁻(aq) → FeS(s)
```
* Reaktion af jern med hydrogensulfid: Når jern reagerer med hydrogensulfid (H2S) gas, dannes jernsulfid sammen med hydrogengas:
```
Fe(s) + H2S(g) → FeS(s) + H₂(g)
```
3. Naturlige forekomster:
* Mineraldannelse: Jernsulfid forekommer naturligt i mineralet pyrit , også kendt som "fool's gold", som er dannet dybt under jorden under højt tryk og temperatur.
* Biogene processer: Nogle bakterier, især dem, der er involveret i anaerob respiration, kan producere ferrosulfid som et biprodukt af deres stofskifte.
4. Industrielle processer:
* Stålproduktion: Under stålproduktionsprocessen kan jernsulfid dannes som et uønsket biprodukt.
* Spildevandsbehandling: Jernsulfid kan bruges i spildevandsrensning for at fjerne tungmetaller som cadmium, bly og kviksølv.
Bemærk: Jernsulfid kan også dannes i andre scenarier, såsom korrosion af jern i miljøer, der indeholder svovlforbindelser.
De specifikke forhold og reaktioner involveret i dannelsen af jernsulfid afhænger af det specifikke miljø og tilstedeværelsen af andre kemiske arter.
 Varme artikler
Varme artikler
-
 Udviklet materiale, der er varmeisolerende og varmeledende på samme tidDet nyudviklede materiale leder varme godt langs lagene, samtidig med at den giver varmeisolering lodret. Kredit:MPI-P, Licens CC-BY-SA. Styrofoam eller kobber - begge materialer har meget forskel
Udviklet materiale, der er varmeisolerende og varmeledende på samme tidDet nyudviklede materiale leder varme godt langs lagene, samtidig med at den giver varmeisolering lodret. Kredit:MPI-P, Licens CC-BY-SA. Styrofoam eller kobber - begge materialer har meget forskel -
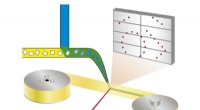 Ny metode muliggør automatiseret hurtig undersøgelse af enzymatiske processerPrincip for bland-og-diffus seriel synkrotronkrystallografi:Proteinkrystaller blandes med en opløsning af en lægemiddelkandidat og røntgenstråles på et bånd, der løber gennem røntgenstrålen. Kredit:Be
Ny metode muliggør automatiseret hurtig undersøgelse af enzymatiske processerPrincip for bland-og-diffus seriel synkrotronkrystallografi:Proteinkrystaller blandes med en opløsning af en lægemiddelkandidat og røntgenstråles på et bånd, der løber gennem røntgenstrålen. Kredit:Be -
 Autonom selvhelbredelse set i piezoelektriske molekylære krystallerKredit:CC0 Public Domain Et team af forskere fra Indian Institute of Science Education and Research i Kolkata, Indian Institute of Technology Kharagpur og RWTH Aachen University, har fundet en typ
Autonom selvhelbredelse set i piezoelektriske molekylære krystallerKredit:CC0 Public Domain Et team af forskere fra Indian Institute of Science Education and Research i Kolkata, Indian Institute of Technology Kharagpur og RWTH Aachen University, har fundet en typ -
 En maskinlæringsløsning til at designe materialer med ønskede optiske egenskaberStyring af lys-stof-interaktioner er central for en række vigtige applikationer, såsom kvantepunkter, som kan bruges som lysgivere og sensorer. Kredit:PlasmaChem At forstå, hvordan stof interagere
En maskinlæringsløsning til at designe materialer med ønskede optiske egenskaberStyring af lys-stof-interaktioner er central for en række vigtige applikationer, såsom kvantepunkter, som kan bruges som lysgivere og sensorer. Kredit:PlasmaChem At forstå, hvordan stof interagere
- Mod en nanomekanisk kvanteomstilling
- USA rapporterer andet menneskeligt tilfælde af fugleinfluenza, der er forbundet med malkekoudbrud
- Smeltevandssøer under det antarktiske indlandsis accelererede istræk i jordens fortid
- Stråler solen synlig og usynlig energi?
- Meiosis er en proces, der producerer hvad?
- Beregning af muldvarpe nødvendige for en kemisk reaktion:En praktisk støkiometriguide


