Kovalente bindinger vs. ioner:Forstå forskellen
* Kovalente bindinger: I en kovalent binding deler atomer elektroner for at opnå en stabil elektronkonfiguration. De overfører ikke elektroner fuldt ud som i ionbindinger.
* ioner: Ioner dannes, når et atom får eller taber elektroner, hvilket resulterer i en netto positiv eller negativ ladning.
Her er den vigtigste forskel:
* ioniske bindinger: Involvere fuldstændig overførsel af elektroner, skabe positivt ladede kationer og negativt ladede anioner.
* Kovalente bindinger: Indebærer deling af elektroner mellem atomer. De delte elektroner tiltrækkes af kernerne i begge atomer og holder dem sammen.
Eksempel:
* Ionisk binding: Natriumchlorid (NaCl). Natrium mister en elektron for at blive en positivt ladet natriumion (Na+), mens klor får en elektron til at blive en negativt ladet chloridion (Cl-). Den elektrostatiske tiltrækning mellem disse modsat ladede ioner danner ionbindingen.
* Kovalent binding: Vand (H2O). Hvert brintatom deler en elektron med oxygenatomet, hvilket skaber et stabilt molekyle uden ioner.
Sammenfattende involverer kovalente bindinger elektrondeling, ikke elektronoverførsel, så de danner ikke ioner.
 Varme artikler
Varme artikler
-
 Brygning af øl, der smager frisk længereKredit:CC0 Public Domain I modsætning til vin, som generelt forbedres med tiden, øl ældes ikke godt. Normalt inden for et år efter aftapning, drikken begynder at udvikle en ubehagelig papiragtig e
Brygning af øl, der smager frisk længereKredit:CC0 Public Domain I modsætning til vin, som generelt forbedres med tiden, øl ældes ikke godt. Normalt inden for et år efter aftapning, drikken begynder at udvikle en ubehagelig papiragtig e -
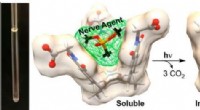 Indfangning af giftige forbindelser med molekylære kurveKredit:Ohio State University Forskere har udviklet designermolekyler, som måske en dag kan opsøge og fange dødelige nervestoffer og andre giftige forbindelser i miljøet – og muligvis i mennesker.
Indfangning af giftige forbindelser med molekylære kurveKredit:Ohio State University Forskere har udviklet designermolekyler, som måske en dag kan opsøge og fange dødelige nervestoffer og andre giftige forbindelser i miljøet – og muligvis i mennesker. -
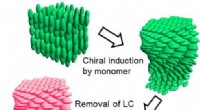 Metode til at skabe optisk aktive polymerer ved hjælp af en spiralformet flydende krystalskabelonGrafisk abstrakt. Kredit:Molekylære krystaller og flydende krystaller (2022). DOI:10.1080/15421406.2022.2073421 En videnskabsmand fra Fakultetet for Rene og Anvendte Videnskaber ved University of T
Metode til at skabe optisk aktive polymerer ved hjælp af en spiralformet flydende krystalskabelonGrafisk abstrakt. Kredit:Molekylære krystaller og flydende krystaller (2022). DOI:10.1080/15421406.2022.2073421 En videnskabsmand fra Fakultetet for Rene og Anvendte Videnskaber ved University of T -
 Byg en 3D-atommodel:En trin-for-trin-vejledning til videnskabsprojekterAf Misty Barton • Opdateret 30. august 2022 I mange naturfagstimer beder lærere eleverne om at konstruere en tredimensionel model af et atom. Denne praktiske aktivitet hjælper eleverne med at forstå
Byg en 3D-atommodel:En trin-for-trin-vejledning til videnskabsprojekterAf Misty Barton • Opdateret 30. august 2022 I mange naturfagstimer beder lærere eleverne om at konstruere en tredimensionel model af et atom. Denne praktiske aktivitet hjælper eleverne med at forstå
- Hvad er en periode fysik?
- Hvorfor kan træ beskrives som en vedvarende energikilde?
- Liste over fisk, der er bundfodere
- Er den følgende sætning sand eller falsk lettet diffusion ikke kræver at bruge energi?
- Ny ORNL-software forbedrer neutronspektroskopidataopløsningen
- Dekonstruerer et mysterium:Hvad forårsagede Snowmaggedon?


