Hvordan opløsningsmidler opløser ioniske forbindelser:En detaljeret forklaring
Her er en oversigt:
* Ioniske forbindelser: Disse forbindelser er sammensat af positivt ladede kationer og negativt ladede anioner holdt sammen af stærke elektrostatiske kræfter.
* Opløsningsmidler: Opløsningsmidler er stoffer, der kan opløse andre stoffer. Polære opløsningsmidler, ligesom vand, har molekyler med en positiv og negativ ende (dipol) på grund af ulige deling af elektroner.
* Opløsningsproces: Når et polært opløsningsmiddel som vand møder en ionisk forbindelse, tiltrækker den positive ende af vandmolekylet de negative ioner (anioner) af den ioniske forbindelse, og den negative ende af vandmolekylet tiltrækker de positive ioner (kationer). Denne tiltrækning svækker de elektrostatiske kræfter, der holder ionerne sammen i det faste stof.
* Hydrering (eller Solvation): Vandmolekylerne omgiver derefter de individuelle ioner og danner en hydreringssfære. Denne proces, kaldet solvation, isolerer effektivt ionerne fra hinanden og forhindrer dem i at gendanne iongitteret. Resultatet er, at den ioniske forbindelse opløses.
Nøglepunkter at huske:
* Polære opløsningsmidler er generelt bedre til at opløse ioniske forbindelser end ikke-polære opløsningsmidler.
* Styrken af de elektrostatiske kræfter mellem ioner i den ioniske forbindelse påvirker dens opløselighed. Stærkere kræfter fører til lavere opløselighed.
* Opløsningsmidlets polaritet påvirker dets evne til at interagere med ionerne og bryde dem fra hinanden.
Sig til, hvis du har andre spørgsmål!
 Varme artikler
Varme artikler
-
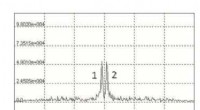 Forskere foreslår en ny metode til at opdage farlige nitrogenholdige væskerNMR -spektrum af mmoniumnitrat. Kredit:Galina Kupriyanova Et team af forskere fra Institut for Fysiske og Matematiske Videnskaber og Informationsteknologier ved Immanuel Kant Baltic Federal Univer
Forskere foreslår en ny metode til at opdage farlige nitrogenholdige væskerNMR -spektrum af mmoniumnitrat. Kredit:Galina Kupriyanova Et team af forskere fra Institut for Fysiske og Matematiske Videnskaber og Informationsteknologier ved Immanuel Kant Baltic Federal Univer -
 Kemikere, der overraskende opdagede nanokonfinerede reaktioner, kunne hjælpe med katalytisk designKredit:Georgia State University Georgia State University kemiforskere har afsløret et af mysterierne bag katalytiske reaktioner i mikroskopisk skala, giver mulighed for design af mere effektive in
Kemikere, der overraskende opdagede nanokonfinerede reaktioner, kunne hjælpe med katalytisk designKredit:Georgia State University Georgia State University kemiforskere har afsløret et af mysterierne bag katalytiske reaktioner i mikroskopisk skala, giver mulighed for design af mere effektive in -
 Knækker mysteriet om naturens hårdeste materialeMeget deformeret og genvundet perlemor. a Skematisk af den indvendige skaloverflade af toskallede bløddyr P. nobilis, med det undersøgte område markeret med en lilla firkant. b HAADF STEM oversigtsbil
Knækker mysteriet om naturens hårdeste materialeMeget deformeret og genvundet perlemor. a Skematisk af den indvendige skaloverflade af toskallede bløddyr P. nobilis, med det undersøgte område markeret med en lilla firkant. b HAADF STEM oversigtsbil -
 En silica nanostruktur med kemo-enzymatisk opdelingElektronmikrografer af SiJAR (til venstre), elektronmikrografer og fluorescensmikrografer af SiJAR-injicerede celler (til højre). Kredit:POSTECH Da COVID-19-vaccinationer er godt i gang, mennesker
En silica nanostruktur med kemo-enzymatisk opdelingElektronmikrografer af SiJAR (til venstre), elektronmikrografer og fluorescensmikrografer af SiJAR-injicerede celler (til højre). Kredit:POSTECH Da COVID-19-vaccinationer er godt i gang, mennesker
- Hvad er en nonfood eller non-beverage brug for svovl?
- En gammel Egypten-til-Sortehavsrute? Eventyrere for at teste teori
- Hvad er dominerende og recessiv?
- Tiltrækningen mellem vandmolekyler er resultatet af vand?
- Hvis et objekt placeres i en flydende oplevelser, den flydende kraft, der er lig med vægten af de…
- Hvad forårsager fotokemisk smog?


