Forstå flere oxidationstilstande:Kan elementer have mere end én?
Her er nogle grunde til, at et grundstof kan have flere oxidationstal:
* Forskellige bindingsmiljøer: Et grundstofs oxidationsnummer kan ændre sig afhængigt af de typer atomer, det er bundet til, og antallet af bindinger, det danner. For eksempel har oxygen i vand (H2O) et oxidationstal på -2, mens det i hydrogenperoxid (H2O2) har et oxidationstal på -1.
* Variabel valens: Nogle elementer kan have flere valenser, hvilket betyder, at de kan danne forskellige antal bindinger. For eksempel kan jern (Fe) have et oxidationstal på +2 i FeCl2 eller +3 i FeCl3.
* Danning af forskellige forbindelser: Det samme grundstof kan deltage i dannelsen af forskellige forbindelser med varierende oxidationstal. For eksempel kan svovl (S) eksistere i forbindelser som H2S (oxidationstal -2), SO2 (oxidationstal +4) og SO3 (oxidationstal +6).
Vigtig bemærkning: Oxidationstal er teoretiske værdier, der bruges til at spore elektronoverførsel i kemiske reaktioner. De repræsenterer ikke altid perfekt de faktiske ladninger på atomer, især i kovalente bindinger.
 Varme artikler
Varme artikler
-
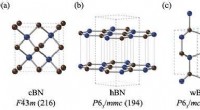 Forudsigelse af den mest stabile bornitridstruktur med kvantesimuleringerStrukturerne og rumgrupperne af (a) zink-blende bornitrid (cBN), (b) hexagonal bornitrid (hBN), (c) wurtzite bornitrid (wBN) og (d) romboedral bornitrid (rBN). Bor- og nitrogenatomer er afbildet i hen
Forudsigelse af den mest stabile bornitridstruktur med kvantesimuleringerStrukturerne og rumgrupperne af (a) zink-blende bornitrid (cBN), (b) hexagonal bornitrid (hBN), (c) wurtzite bornitrid (wBN) og (d) romboedral bornitrid (rBN). Bor- og nitrogenatomer er afbildet i hen -
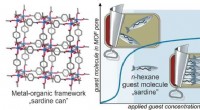 Gæstejustering og defektdannelse under porefyldning i metal-organiske rammefilmDen metalorganiske ramme danner et stillads med nanometerstore porer, som holder molekyler (til venstre). Så længe n-hexangas-molekyler tilsættes til porerne under tryk, justeres molekylerne i en sard
Gæstejustering og defektdannelse under porefyldning i metal-organiske rammefilmDen metalorganiske ramme danner et stillads med nanometerstore porer, som holder molekyler (til venstre). Så længe n-hexangas-molekyler tilsættes til porerne under tryk, justeres molekylerne i en sard -
 Sikker fremtid for jernbanetransport af farlige materialer under udviklingHota GangaRao, Maurice A. og JoAnn Wadsworth Department of Civil and Environmental Engineering og direktør for Constructed Facilities Center, i et laboratorium. Det nyinnoverede kompositmateriale, der
Sikker fremtid for jernbanetransport af farlige materialer under udviklingHota GangaRao, Maurice A. og JoAnn Wadsworth Department of Civil and Environmental Engineering og direktør for Constructed Facilities Center, i et laboratorium. Det nyinnoverede kompositmateriale, der -
 Ingeniører kan opdage ultra sjældne proteiner i blodet ved hjælp af et mobiltelefonkameraForskernes detektionssystem bruger et standard mobiltelefonkamera til at optage video af mikrodråber, når de passerer linsen. Fluorescerende markører kan identificeres individuelt ved at matche dem me
Ingeniører kan opdage ultra sjældne proteiner i blodet ved hjælp af et mobiltelefonkameraForskernes detektionssystem bruger et standard mobiltelefonkamera til at optage video af mikrodråber, når de passerer linsen. Fluorescerende markører kan identificeres individuelt ved at matche dem me
- Positionens energi er hvilken slags energi?
- Den længste lige streg havstrækning på planeten Jorden beregnet
- Styrer dyr jordens iltniveau?
- Hvordan opbevares energikilden, når den er kommet sig i olie?
- Forskere forbedrer den termiske ledningsevne af almindelig plast ved at tilføje grafenbelægning
- Dendrit-sikre batterier muliggjort af Zylon nanofibre


