Cp - Cv =R:Hvorfor det ikke gælder for faste stoffer og væsker
* Ideel gasantagelse: Denne ligning er afledt af den ideelle gaslov og dens antagelser. En central antagelse er, at det eneste arbejde, der udføres af gassen, er tryk-volumen arbejde. Det betyder, at gassens indre energi udelukkende er afhængig af dens temperatur.
* Faststoffer og væsker: I modsætning hertil har faste stoffer og væsker meget stærkere intermolekylære kræfter og er mere tætpakket.
* Kompressibilitet: Faste stoffer og væsker er mindre komprimerbare end gasser. Det betyder, at ændringer i tryk har en meget mindre indflydelse på deres volumen.
* Intern energi: Den indre energi af faste stoffer og væsker er ikke udelukkende bestemt af temperaturen. Det inkluderer også bidrag fra molekylære vibrationer, rotationer og interaktioner mellem molekyler.
Nøgleforskelle:
* Cv: Varmekapaciteten ved konstant volumen (Cv) måler den energi, der kræves for at hæve et stofs temperatur med 1 grad Celsius, mens volumenet holdes konstant. Dette svarer til gasser, faste stoffer og væsker.
* Cp: Varmekapaciteten ved konstant tryk (Cp) måler den energi, der kræves for at hæve temperaturen på et stof med 1 grad Celsius, mens trykket holdes konstant.
* For faste stoffer og væsker er Cp typisk *lidt* større end Cv, fordi der bruges noget energi til at arbejde mod trykket, da volumenet udvider sig en smule. Forskellen er dog meget mindre end R-værdien.
Som konklusion: Cp - Cv =R forholdet er en konsekvens af den ideelle gaslov og dens antagelser om arten af gasmolekyler. Dette forhold gælder ikke for faste stoffer og væsker på grund af deres forskellige molekylære interaktioner, kompressibiliteter og interne energibidrag.
Sidste artikelOxidationstal af propan (C3H8):En klar forklaring
Næste artikelSaltsyre vs. Eddikesyre:Styrke og egenskaber forklaret
 Varme artikler
Varme artikler
-
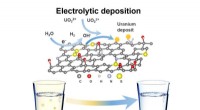 Brug af grafenskum til at filtrere toksiner fra drikkevandEt genanvendeligt 3D-funktionaliseret reduceret grafenoxidskum (3D-FrGOF) bruges som en in situ elektrolytisk aflejringselektrode til at udvinde uran fra forurenet vand. Kredit:MIT Nogle former fo
Brug af grafenskum til at filtrere toksiner fra drikkevandEt genanvendeligt 3D-funktionaliseret reduceret grafenoxidskum (3D-FrGOF) bruges som en in situ elektrolytisk aflejringselektrode til at udvinde uran fra forurenet vand. Kredit:MIT Nogle former fo -
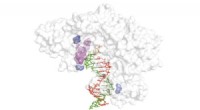 En ny rettet evolutionsteknik til at frigøre potentialet for xeno-nukleinsyrerDiagram, der viser den omvendte transkriptasestruktur (hvid) med spirende cDNA -streng (rød), XNA -skabelon (grøn) og områder kritiske for omvendt transkription af XNA -skabeloner (blå og lilla). Kred
En ny rettet evolutionsteknik til at frigøre potentialet for xeno-nukleinsyrerDiagram, der viser den omvendte transkriptasestruktur (hvid) med spirende cDNA -streng (rød), XNA -skabelon (grøn) og områder kritiske for omvendt transkription af XNA -skabeloner (blå og lilla). Kred -
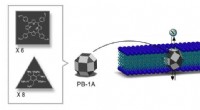 Syntetiske nanokanaler til jodidtransport3-D struktur af den syntetiske iodid-transporter PB-1A udviklet af IBS forskere. PB-1A-design følger formen af 26-sidet polyeder lavet af trekanter og firkanter (mørkegrå) med 12 flader efterladt to
Syntetiske nanokanaler til jodidtransport3-D struktur af den syntetiske iodid-transporter PB-1A udviklet af IBS forskere. PB-1A-design følger formen af 26-sidet polyeder lavet af trekanter og firkanter (mørkegrå) med 12 flader efterladt to -
 Højteknologisk sensing belyser betonstresstestEt billede fra et fotonisk kamera, der viser, hvordan brug af belægningen kan skabe en stearinlyslignende flamme, der fremhæver forskydningsspændingsfordelingen i en prøvebetonbjælke. Kredit:Universit
Højteknologisk sensing belyser betonstresstestEt billede fra et fotonisk kamera, der viser, hvordan brug af belægningen kan skabe en stearinlyslignende flamme, der fremhæver forskydningsspændingsfordelingen i en prøvebetonbjælke. Kredit:Universit
- Livet gik bare galt:Hvorfor militærveteraner er dobbelt så tilbøjelige til at ende i fængsel
- Kraftige emissioner skal elimineres for at standse klimaændringer, anmeldelse viser
- Vil siliciumnitrid og almindelig kemi hjælpe med at revolutionere genomisk sekventering?
- Hvordan er masse relateret til Newtons 1. lov?
- Små kredsløb, lange afstande:Mindre lysbehandlingsenheder til fiberoptisk kommunikation
- Hvordan husdyrsystemer fungerer som et reservoir for antimikrobielle resistente bakterier


