Oxidationstal af propan (C3H8):En klar forklaring
Her er hvorfor:
* Oxidationstal repræsenterer den hypotetiske ladning et atom ville have, hvis alle bindinger var ioniske.
* I et neutralt molekyle skal summen af alle atomers oxidationstal være lig med nul.
* Brint har typisk et oxidationstal på +1.
* Kulstof har et variabelt oxidationstal, men i kulbrinter er det typisk -3.
Lad os beregne oxidationstallet for kulstof i propan:
* 3 carbonatomer * x (oxidationstal af carbon) + 8 hydrogenatomer * (+1) =0
* 3x + 8 =0
* 3x =-8
* x =-8/3
Da vi ikke kan have fraktionerede oxidationstal, kan vi sige, at det gennemsnitlige oxidationstal for kulstof i propan er -3 .
Vigtig bemærkning: Mens det gennemsnitlige oxidationstal af kulstof i propan er -3, betyder det ikke, at hvert kulstofatom individuelt har et -3 oxidationstal. Oxidationstallene er tildelt baseret på elektronegativitetsforskelle, og bindingerne i propan har en vis kovalent karakter.
 Varme artikler
Varme artikler
-
 Sådan forbereder du en højkvalitets elektrolytløsning til batterierAf Sean Lancaster Opdateret 24. marts 2022 Batterier er afhængige af to halvcelle-reaktioner, der er forbundet med en saltbro og nedsænket i en elektrolytopløsning. Blysyrebatteriet, en fast bestand
Sådan forbereder du en højkvalitets elektrolytløsning til batterierAf Sean Lancaster Opdateret 24. marts 2022 Batterier er afhængige af to halvcelle-reaktioner, der er forbundet med en saltbro og nedsænket i en elektrolytopløsning. Blysyrebatteriet, en fast bestand -
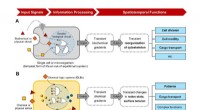 Udforskning af kemiske logiske systemer, der kan reagere på miljøforholdSensing, informationsbehandling og generering af programmerbare funktioner. Skematisk repræsentation af boolsk logik regulerede spatiotemporale funktioner i ude af ligevægt i (A) et levende system (en
Udforskning af kemiske logiske systemer, der kan reagere på miljøforholdSensing, informationsbehandling og generering af programmerbare funktioner. Skematisk repræsentation af boolsk logik regulerede spatiotemporale funktioner i ude af ligevægt i (A) et levende system (en -
 Beregning af varmeenergi i joule:en praktisk vejledningAf John Brennan, Opdateret 24. marts 2022 I begyndelsen af det 19. århundrede demonstrerede den britiske brygger og fysiker JamesJoule, at varme og mekanisk arbejde er to udtryk for den samme energi.
Beregning af varmeenergi i joule:en praktisk vejledningAf John Brennan, Opdateret 24. marts 2022 I begyndelsen af det 19. århundrede demonstrerede den britiske brygger og fysiker JamesJoule, at varme og mekanisk arbejde er to udtryk for den samme energi. -
 Kemikalier bag øjeblikkelige ispakker:Sådan fungerer deAf Michael Hinckley Opdateret 24. marts 2022 Øjeblikkelige isposer er en fast bestanddel i førstehjælpskasser, der tilbyder hurtig kuldebehandling ved forstuvninger, forstrækninger og mindre skader.
Kemikalier bag øjeblikkelige ispakker:Sådan fungerer deAf Michael Hinckley Opdateret 24. marts 2022 Øjeblikkelige isposer er en fast bestanddel i førstehjælpskasser, der tilbyder hurtig kuldebehandling ved forstuvninger, forstrækninger og mindre skader.


