Sådan forbereder du en højkvalitets elektrolytløsning til batterier
Af Sean Lancaster
Opdateret 24. marts 2022
Batterier er afhængige af to halvcelle-reaktioner, der er forbundet med en saltbro og nedsænket i en elektrolytopløsning. Blysyrebatteriet, en fast bestanddel i bilkraftsystemer, bruger blydioxid og brint-halvceller. Elektrolytten - typisk en blanding af svovlsyre og vand - giver de sulfationer, der er nødvendige for iltudvikling og fungerer som en ladningsbærer mellem elektroderne.
Trin 1:Brug rent vand
Fyld et bægerglas cirka halvt med destilleret vand. Destilleret vand minimerer forurenende stoffer, der kan forstyrre iontransport. For eksempel kan spor af bly i postevand udfældes, når det blandes med NaCl, hvilket ændrer opløsningens ledningsevne.
Trin 2:Vælg den rigtige elektrolyt
Vælg en elektrolyt, der komplementerer kemien i dit batteris halvceller. Hvis kobber er involveret, er CuCO₃ eller CuCl₂ passende, fordi de giver Cu²+-ioner. Generelt foretrækkes en stærk syre, stærk base eller deres salte – såsom H₂SO4, NaOH eller Na₂SO4 – på grund af deres høje dissociationshastigheder og effektive ladningstransport.
Trin 3:Bestem koncentrationen
Mål nok elektrolyt til at opnå en koncentration omkring 1M. Koncentrationer under denne tærskel kan begrænse cellens ydeevne, mens en for høj koncentration kan forårsage for høj viskositet eller ætsende skade.
Trin 4:Bland og omrør
Hæld den målte elektrolyt i bægeret med destilleret vand. Rør grundigt med en ren stang, indtil opløsningen er homogen. Dette sikrer ensartet ionfordeling og optimal ledningsevne.
Nødvendige materialer
- Bægerglas
- Stærk syre, base eller salt (f.eks. H₂SO4, NaOH, Na₂SO4)
- Destilleret vand
- Rørestang
 Varme artikler
Varme artikler
-
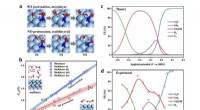 Forskere afslører potentiel afhængighed af nitrogenoxid -elektrisk reduktion til ammoniak(a)-(b) Verifikation af monolagsvandmodel i elektrokatalytiske energibarriereberegninger; (c)-(d) Sammenligning af teoretisk og eksperimentel faradaisk effektivitet. Kredit:LONG Jun Kvælstofoxid (
Forskere afslører potentiel afhængighed af nitrogenoxid -elektrisk reduktion til ammoniak(a)-(b) Verifikation af monolagsvandmodel i elektrokatalytiske energibarriereberegninger; (c)-(d) Sammenligning af teoretisk og eksperimentel faradaisk effektivitet. Kredit:LONG Jun Kvælstofoxid ( -
 Enhed, der anvender molekylær teknik, kunne give ultrafølsomme, automatiseret system til at opdage…Jacqueline Linnes, en assisterende professor ved Purdues Weldon School of Biomedical Engineering, udvikler nukleinsyreamplifikationstest trykt på papir for at muliggøre en lav pris, automatiseret syst
Enhed, der anvender molekylær teknik, kunne give ultrafølsomme, automatiseret system til at opdage…Jacqueline Linnes, en assisterende professor ved Purdues Weldon School of Biomedical Engineering, udvikler nukleinsyreamplifikationstest trykt på papir for at muliggøre en lav pris, automatiseret syst -
 Billeder af usynlige huller på celler kan sætte gang i forskningenSeks mikroskopiske billeder af 3D-poreproteinet pannexin 1. Billederne blev optaget ved hjælp af kryo-elektronmikroskopi. Hvert poreprotein er omkring 6 nm bredt. Det betyder, at godt 300, 000 kunne p
Billeder af usynlige huller på celler kan sætte gang i forskningenSeks mikroskopiske billeder af 3D-poreproteinet pannexin 1. Billederne blev optaget ved hjælp af kryo-elektronmikroskopi. Hvert poreprotein er omkring 6 nm bredt. Det betyder, at godt 300, 000 kunne p -
 Ulovlig stofbrug kan være højere end hidtil antaget; svæver under særlige begivenhederKredit:CC0 Public Domain Amerikas narkotikaproblem kan være endnu værre, end embedsmænd er klar over. Og ulovlige stoffer indtages i højere grad under festlige begivenheder. Det er blot to af de k
Ulovlig stofbrug kan være højere end hidtil antaget; svæver under særlige begivenhederKredit:CC0 Public Domain Amerikas narkotikaproblem kan være endnu værre, end embedsmænd er klar over. Og ulovlige stoffer indtages i højere grad under festlige begivenheder. Det er blot to af de k
- Når ATP frigiver lidt energi, det også uorganisk fosfat hvilket formål tjener dette i cellen?
- Er eddike og olie en blanding?
- Hvad undersøgelser af børns holdninger kan fortælle os om kønsbaseret lønulighed
- Hvordan bruger du en pære sifon?
- Spørgsmål og svar:Det kritiske behov for at adressere kemisk forurening i drikkevand
- Sammenlign og kontrast dyreceller planter eukaryote prokaryoteceller?


