Beregning af varmeenergi i joule:en praktisk vejledning
Af John Brennan, Opdateret 24. marts 2022
I begyndelsen af det 19. århundrede demonstrerede den britiske brygger og fysiker JamesJoule, at varme og mekanisk arbejde er to udtryk for den samme energi. Hans indsigt skaffede ham en varig plads i videnskaben; i dag er enheden til måling af energi og varme opkaldt efter ham.
Du kan nemt beregne mængden af varme, der absorberes eller frigives af en genstand, hvis du kender dens masse, temperaturændringen og materialets specifikke varmekapacitet.
Billedkredit:RazoomGames/iStock/GettyImages
TL;DR
Varme (i joule) =masse × ΔT × specifik varmekapacitet.
1. Find den specifikke varmekapacitet
Slå op på den specifikke varmekapacitet af dit materiale. Almindelige tabeller viser værdier i kJ/kgK (kJ =kilojoule, kg =kilogram, K =Kelvin). En grad Kelvin er lig med en grad Celsius.
2. Bestem temperaturændringen
Træk starttemperaturen fra sluttemperaturen. Hvis ændringen er angivet i Fahrenheit, konverter den til Celsius med (°F – 32) × 5⁄9 =°C og tilføj derefter 273,15 for at opnå Kelvin.
3. Udfør beregningen
Multiplicer temperaturændringen med den specifikke varmekapacitet og massen for at opnå varmevekslet i joule.
Eksempel: 10 kg vand opvarmet fra 10°C til 50°C.
Specifik varme af vand ≈ 4,184kJ/kgK.
Varme =10kg × 40°C × 4,184kJ/kgK =1673,6kJ (≈1,67MJ).
Nødvendige værktøjer
- Blyant
- Papir
- Lommeregner
 Varme artikler
Varme artikler
-
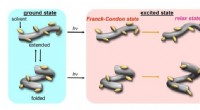 Under tryk:Manipulering af protein-efterlignende molekyler med hydrostatisk trykI grundtilstanden, værten vedtager to konformere, en forlænget og en foldet, og gradvist skifter til en udvidet-rig tilstand efter tryk. Derefter, i ophidset tilstand (hυ), disse to konformere udsende
Under tryk:Manipulering af protein-efterlignende molekyler med hydrostatisk trykI grundtilstanden, værten vedtager to konformere, en forlænget og en foldet, og gradvist skifter til en udvidet-rig tilstand efter tryk. Derefter, i ophidset tilstand (hυ), disse to konformere udsende -
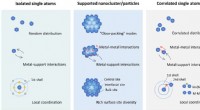 Nye elektrokatalysatorer varsler kulstofneutralitetC-SACer med metal-metal interaktioner. Sammenligning af C-SACer med de konventionelle isolerede SACer og understøttede metalliske klynge/nanopartikelkatalysatorer fra perspektivet af rumlig fordeling,
Nye elektrokatalysatorer varsler kulstofneutralitetC-SACer med metal-metal interaktioner. Sammenligning af C-SACer med de konventionelle isolerede SACer og understøttede metalliske klynge/nanopartikelkatalysatorer fra perspektivet af rumlig fordeling, -
 Kumarinforbindelser fra egetræsfade kunne bidrage til bitter smag i vin og spiritusKredit:Pixabay/CC0 Public Domain Vin og spiritus er komplekse blandinger af smags- og aromaforbindelser, hvoraf nogle opstår under lagring i træfade. Blandt andre forbindelser, egetræ frigiver kum
Kumarinforbindelser fra egetræsfade kunne bidrage til bitter smag i vin og spiritusKredit:Pixabay/CC0 Public Domain Vin og spiritus er komplekse blandinger af smags- og aromaforbindelser, hvoraf nogle opstår under lagring i træfade. Blandt andre forbindelser, egetræ frigiver kum -
 Trin-for-trin guide til beregning af molekylær polaritetAf David Ward Opdateret 24. marts 2022 En kemiker kan ofte forudsige, om et molekyle er polært ved at overveje elektronegativiteten af dets konstituerende atomer. Men en præcis bestemmelse af et mole
Trin-for-trin guide til beregning af molekylær polaritetAf David Ward Opdateret 24. marts 2022 En kemiker kan ofte forudsige, om et molekyle er polært ved at overveje elektronegativiteten af dets konstituerende atomer. Men en præcis bestemmelse af et mole
- Arabisk rumfartøj lukker ind på Mars på en historisk flyvning
- Cool 7th Grade Science Experiments
- En ny tilgang til at lægge et svært kræftmål
- Adskillelse af ølaffald til proteiner til fødevarer, og fiber til biobrændstoffer
- Er det sandt, at de fleste arter kun kan overleve og gengive i et miljø med abiotiske faktorer inde…
- Sådan fungerer vinfremstilling


