Forståelse af ionisk opløsning:Hvorfor salte opløses i vand
1. Polaritet og tiltrækning
* Vand er et polært molekyle: Iltatomet i vand har en svagt negativ ladning, mens brintatomerne har en svagt positiv ladning. Dette skaber et dipolmoment.
* Ioniske forbindelser er lavet af ioner: De består af positivt ladede kationer og negativt ladede anioner, der holdes sammen af elektrostatiske kræfter.
* Tiltrækning mellem vand og ioner: De positive ender af vandmolekyler (brintatomer) tiltrækkes af de negativt ladede anioner i den ioniske forbindelse. På samme måde bliver de negative ender af vandmolekyler (iltatomer) tiltrukket af de positivt ladede kationer.
2. Opløsningsprocessen
1. Hydrering: Når en ionforbindelse anbringes i vand, omgiver vandmolekyler ionerne og danner hydreringsskaller. Tiltrækningskræfterne mellem vandmolekylerne og ionerne er stærkere end de kræfter, der holder ionerne sammen i krystalgitteret.
2. Adskillelse: Tiltrækningen mellem vandmolekylerne og ionerne overvinder de ioniske bindinger, der holder forbindelsen sammen, hvilket får ionerne til at adskille og spredes i vandet.
3. Opløsning: Resultatet er dannelsen af en opløsning, hvor ionerne er omgivet af vandmolekyler, der effektivt opløser den ioniske forbindelse.
3. Faktorer, der påvirker opløselighed
* Opladningstæthed: Ioner med højere ladningstæthed (større ladning i et mindre volumen) har stærkere tiltrækningskraft med vandmolekyler, hvilket fører til større opløselighed.
* Gitterenergi: Styrken af ionbindingerne i krystalgitteret påvirker opløseligheden. Forbindelser med svagere gitterenergi er mere tilbøjelige til at opløses.
* Temperatur: Opløseligheden af de fleste ioniske forbindelser stiger med temperaturen, da den øgede kinetiske energi hjælper med at overvinde tiltrækningerne mellem ioner i det faste stof.
Opsummering: Ioniske forbindelser opløses i vand, fordi den stærke tiltrækning mellem vandmolekyler og ionerne overvinder de elektrostatiske kræfter, der holder ionerne sammen i krystalgitteret. Denne proces involverer dannelsen af hydreringsskaller omkring ionerne og den efterfølgende adskillelse og dispergering af ioner i vandet.
Sidste artikelForståelse af kemiske formler:Symboler for forbindelser
Næste artikelDestilleret vand:Forståelse af pH og neutralitet
 Varme artikler
Varme artikler
-
 Kulstof nanorør efterligner biologiEn kunstners gengivelse af et kulstofnanorør-porin indlejret i en cellemembran med en enkelt DNA-streng, der passerer gennem den. Kredit:Adam Gardner Proteiner i lipidmembraner er en af de grund
Kulstof nanorør efterligner biologiEn kunstners gengivelse af et kulstofnanorør-porin indlejret i en cellemembran med en enkelt DNA-streng, der passerer gennem den. Kredit:Adam Gardner Proteiner i lipidmembraner er en af de grund -
 At få dufte til at vare længereEn sensor, der normalt bruges i fødevareindustrien, kan registrere, hvor længe dufte varer på huden. Kredit:Ashland Fra blomsterparfume til frugtagtig kropsvask og shampoo, dufte har stor indflyde
At få dufte til at vare længereEn sensor, der normalt bruges i fødevareindustrien, kan registrere, hvor længe dufte varer på huden. Kredit:Ashland Fra blomsterparfume til frugtagtig kropsvask og shampoo, dufte har stor indflyde -
 Forskning guider fremtiden for kemisk genanvendelse af plastaffaldKredit:CC0 Public Domain Ny forskning fra Cornell College of Engineering har til formål at lette processen med kemisk genanvendelse - en ny industri, der kunne gøre affaldsprodukter tilbage til na
Forskning guider fremtiden for kemisk genanvendelse af plastaffaldKredit:CC0 Public Domain Ny forskning fra Cornell College of Engineering har til formål at lette processen med kemisk genanvendelse - en ny industri, der kunne gøre affaldsprodukter tilbage til na -
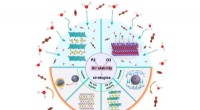 Luftstabilitet af natriumbaserede lagdelte oxidkatodematerialerAdskillige mekanismer og strategier blev vist i denne graf vedrørende luftfølsomheden af lagdelte natriumkatodematerialer. Kredit:Science China Press Natrium-ion-batterier anses for at være et af
Luftstabilitet af natriumbaserede lagdelte oxidkatodematerialerAdskillige mekanismer og strategier blev vist i denne graf vedrørende luftfølsomheden af lagdelte natriumkatodematerialer. Kredit:Science China Press Natrium-ion-batterier anses for at være et af
- Er det sandt, at vinde ikke kan sprænge mod tyngdekraften?
- Cambrian Sixtymile Formation of Grand Canyon giver nye resultater
- Fossile brændstoffer:Sådan lagres sollysets energi
- Hvad er den 2. hotteste planet i solsystemet?
- Dyre- vs. planteceller:Forståelse af nettobevægelsesforskelle
- Hvilken type blad ville være bedst egnet til et meget solrigt klima, og hvorfor?


