Metaller mere reaktive end aluminium med saltsyre:En reaktivitetsserieanalyse
Reaktivitetsserie
Reaktivitetsserien er et diagram, der rangerer metaller fra mest reaktive til mindst reaktive. Metaller højere i serien vil reagere kraftigere med syrer som HCl.
* Metaller mere reaktive end aluminium:
* Lithium (Li): Reagerer meget voldsomt med HCl og danner brintgas og lithiumchlorid. Reaktionen er ofte eksplosiv.
* Natrium (Na): I lighed med lithium reagerer natrium eksplosivt med HCl.
* Kalium (K): Reagerer ekstremt voldsomt med HCl og producerer varme og brintgas.
* Calcium (Ca): Reagerer kraftigt med HCl og danner hydrogengas og calciumchlorid.
* Magnesium (Mg): Reagerer med HCl for at producere hydrogengas og magnesiumchlorid. Reaktionen er mærkbart kraftigere end aluminium.
Hvorfor aluminium er mindre reaktivt:
Aluminium er et reaktivt metal, men det danner et tyndt, beskyttende oxidlag (aluminiumoxid) på overfladen. Dette lag fungerer som en barriere, der bremser reaktioner med syrer.
Nøglepunkter:
* Syrekoncentration: Koncentrationen af saltsyren påvirker også reaktionshastigheden. Mere koncentreret HCl vil føre til hurtigere reaktioner.
* Temperatur: Højere temperaturer øger reaktionshastigheden, inklusive dem, der involverer metaller og syrer.
Sikkerhed:
* Håndter altid stærke syrer med ekstrem forsigtighed.
* Bær passende sikkerhedsudstyr (handsker, beskyttelsesbriller, laboratoriefrakke).
* Udfør reaktioner i et godt ventileret område.
* Føj aldrig vand til syre. Reaktionen kan være eksoterm og farlig.
Lad mig vide, hvis du har andre spørgsmål om metalreaktivitet!
Sidste artikelElementer vs. molekyler:Forståelse af stoffets byggesten
Næste artikelSaltsyre (HCl):Egenskaber, anvendelser og sikkerhed
 Varme artikler
Varme artikler
-
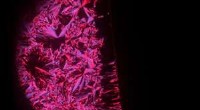 At bryde symmetri fører til responsive organiske fotodetektorerEt polariseret optisk mikroskopibillede af de søjleformede flydende krystaller klemt mellem to krydsede polarisatorer med (højre) og uden (venstre) et elektrisk felt. Dette tyder på, at anvendelse af
At bryde symmetri fører til responsive organiske fotodetektorerEt polariseret optisk mikroskopibillede af de søjleformede flydende krystaller klemt mellem to krydsede polarisatorer med (højre) og uden (venstre) et elektrisk felt. Dette tyder på, at anvendelse af -
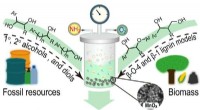 Ny strategi muliggør successiv spaltning og funktionalisering af C–C-bindinger i alkoholerSkematiske illustrationer af manganoxid til katalytisk spaltning og funktionalisering af alkoholreaktion. Kredit:He Peipei Et forskerhold ledet af prof. Dai Wen fra Dalian Institute of Chemical Phy
Ny strategi muliggør successiv spaltning og funktionalisering af C–C-bindinger i alkoholerSkematiske illustrationer af manganoxid til katalytisk spaltning og funktionalisering af alkoholreaktion. Kredit:He Peipei Et forskerhold ledet af prof. Dai Wen fra Dalian Institute of Chemical Phy -
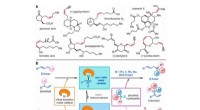 Iridium-katalyserede Z-tilbageholdende asymmetriske allyliske substitutionsreaktionerStrategi for konstruktion af Z-olefiner via asymmetriske allyliske substitutionsreaktioner katalyseret af overgangsmetalkatalysatorer. (A) Udvalgte naturlige produkter indeholdende Z-olefiner med homo
Iridium-katalyserede Z-tilbageholdende asymmetriske allyliske substitutionsreaktionerStrategi for konstruktion af Z-olefiner via asymmetriske allyliske substitutionsreaktioner katalyseret af overgangsmetalkatalysatorer. (A) Udvalgte naturlige produkter indeholdende Z-olefiner med homo -
 Forskere udvikler en meget følsom molekylær optisk tryksensorDen molekylære rubin i fast (rød) og opløst (gul) tilstand kan bruges til kontaktløs optisk måling af tryk. Kredit:Sven Otto, JGU Kemikere ved Johannes Gutenberg University Mainz (JGU) og ved Univ
Forskere udvikler en meget følsom molekylær optisk tryksensorDen molekylære rubin i fast (rød) og opløst (gul) tilstand kan bruges til kontaktløs optisk måling af tryk. Kredit:Sven Otto, JGU Kemikere ved Johannes Gutenberg University Mainz (JGU) og ved Univ
- Twisty-fotoner kunne sætte turbo på næste generations kvantekommunikation
- Bruxelles overvejer skat på bilbrug for at reducere trafikpropper
- Rumalderen for metaller, skum og det levende
- Dark Alliance-videospil fra 2020'erne byder på ikoniske Dungeons &Dragons-karakterer, Beliggenhed
- Toyotas humanoid duplikerer bevægelser i robotisk mobilitet
- Hvad er de sammensatte formuler til natriumphosphat?


