Stærke vs. svage syrer:Forstå de vigtigste forskelle
Stærke syrer
* Fuldstændig ionisering: Når stærke syrer opløses i vand, ioniseres de *fuldstændigt* (brækkes fra hinanden) til hydrogenioner (H+) og deres tilsvarende anioner. Det betyder, at næsten alle syremolekylerne donerer deres proton (H+) til vandmolekyler.
* Høj koncentration af H+ ioner: På grund af fuldstændig ionisering har stærke syrer en meget høj koncentration af H+ ioner i opløsning. Dette fører til en lav pH (meget sur).
* Eksempler: Saltsyre (HCl), svovlsyre (H2SO4), salpetersyre (HNO3), perchlorsyre (HClO4)
Svage syrer
* Delvis ionisering: Svage syrer ioniseres kun delvist i opløsning. De fleste af syremolekylerne forbliver i deres oprindelige form, og kun en lille del donerer deres proton til vand.
* Lavere koncentration af H+ ioner: På grund af delvis ionisering har svage syrer en lavere koncentration af H+ ioner i opløsning sammenlignet med stærke syrer. Dette resulterer i en højere pH (mindre sur).
* Ligevægt: Ioniseringen af svage syrer er en ligevægtsreaktion. Det betyder, at syremolekylerne konstant donerer og accepterer protoner, hvor ligevægten ligger tungt mod den udissocierede syre.
* Eksempler: Eddikesyre (CH₃COOH), kulsyre (H₂CO₃), flussyre (HF)
Nøgleforskelle i en nøddeskal
| Funktion | Stærke syrer | Svage syrer |
|--------------|----------------------------------------------------------------------------------------------------------------|
| Ionisering | Komplet | Delvis |
| H+ Koncentration | Høj | Lav |
| pH | Lav (meget sur) | Højere (mindre surt) |
| Ligevægt | Ikke relevant, i det væsentlige fuldstændig ionisering | Ja, ligevægt mellem ioniseret og ikke-ioniseret |
Vigtig bemærkning: Udtrykkene "stærk" og "svag" henviser til *omfanget* af ionisering i opløsning, ikke koncentrationen af syren. En fortyndet opløsning af en stærk syre kan stadig være meget sur.
 Varme artikler
Varme artikler
-
 Hvad afslører abonnementer i kemiske formler?jittawit.21/iStock/GettyImages I hvert kemipensum kondenserer kemiske formler kompleks information til en kompakt notation. Subskripter, der ofte overses, er afgørende – de dikterer den præcise samme
Hvad afslører abonnementer i kemiske formler?jittawit.21/iStock/GettyImages I hvert kemipensum kondenserer kemiske formler kompleks information til en kompakt notation. Subskripter, der ofte overses, er afgørende – de dikterer den præcise samme -
 Ny proces til fremstilling af højspændingskatoder til lithium-ion-batterierDr. Jennifer Ludwig ved det tekniske universitet i München (TUM) har udviklet en proces, der tillader en hurtig, enkel, og omkostningseffektiv produktion af nanokrystallinske lithiumkoboltphosphatkrys
Ny proces til fremstilling af højspændingskatoder til lithium-ion-batterierDr. Jennifer Ludwig ved det tekniske universitet i München (TUM) har udviklet en proces, der tillader en hurtig, enkel, og omkostningseffektiv produktion af nanokrystallinske lithiumkoboltphosphatkrys -
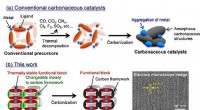 En ny synteserute for alternative katalysatorer af ædelmetallerSynteseskemaer af (a) konventionelle carbonholdige katalysatorer og (b) dette arbejde for ordnede carbonholdige rammer. Kredit:Hirotomo Nishihara Forskere har udviklet en ny synteserute for altern
En ny synteserute for alternative katalysatorer af ædelmetallerSynteseskemaer af (a) konventionelle carbonholdige katalysatorer og (b) dette arbejde for ordnede carbonholdige rammer. Kredit:Hirotomo Nishihara Forskere har udviklet en ny synteserute for altern -
 Bevarelse af masse:Hvordan afbalancering af kemiske ligninger demonstrerer en grundlæggende lovDragonImages/iStock/GettyImages Bevarelse af messen:Grundloven Bevarelsen af masse siger, at den samlede masse i et lukket system forbliver konstant - stof kan ikke skabes eller ødelægges under en ke
Bevarelse af masse:Hvordan afbalancering af kemiske ligninger demonstrerer en grundlæggende lovDragonImages/iStock/GettyImages Bevarelse af messen:Grundloven Bevarelsen af masse siger, at den samlede masse i et lukket system forbliver konstant - stof kan ikke skabes eller ødelægges under en ke
- Hvorfor bruger du reostat på 15 ohm modstand i eksperimentet?
- Intonationen biraciale mænd bruger ændringer, når de taler om race
- Hvad er det lille glasplads, der går på vådmonteringsglas?
- Hvilken egenskab har væsker og gasser, som faste stoffer ikke har?
- Indiens højesteret forbyder beskidt brændstof for at bekæmpe Delhis dårlige luft
- Hvilke videnskabelige opdagelser blev gjort i 1700'erne?


