Forståelse af atom- og molekylær bevægelse:Kinetisk teori forklaret
* De er konstant i bevægelse. Dette er kendt som den kinetiske molekylære teori. Selv i faste stoffer vibrerer atomer og molekyler.
* Mængden af bevægelse afhænger af temperaturen. Højere temperaturer betyder hurtigere bevægelse. Tænk på, hvordan en varm kop te damper (vandmolekyler, der slipper ud) sammenlignet med en kold kop.
* Bevægelsestypen afhænger af stoffets tilstand.
* Fast: Atomer og molekyler vibrerer i faste positioner.
* Væsker: Atomer og molekyler kan bevæge sig mere frit rundt om hinanden, men de er stadig relativt tæt på hinanden.
* Gasser: Atomer og molekyler bevæger sig hurtigt rundt og er langt fra hinanden.
* Bevægelse påvirker mange fysiske egenskaber:
* Temperatur: Højere bevægelse betyder højere temperatur.
* Diffusion: Bevægelse får molekyler til at sprede sig, hvilket fører til diffusion (som en dråbe madfarve, der spredes i vand).
* Tryk: Gasmolekylernes kollisioner med væggene i en beholder skaber tryk.
* Kollisioner: Atomer og molekyler kolliderer konstant med hinanden. Disse kollisioner kan overføre energi.
* Bevægelse er tilfældig: Mens der er tendenser i bevægelse baseret på stoftilstand og temperatur, er den individuelle bevægelse af atomer og molekyler tilfældig.
Opsummeret er bevægelsen af atomer og molekyler fundamental for vores forståelse af stof og dets egenskaber.
Sidste artikelMagnesiumcarbonat og svovlsyrereaktion:ligning og produkter
Næste artikelAtomer vs. Molecules:Forståelse af stoffets byggesten
 Varme artikler
Varme artikler
-
 Hvordan katteurt gør det kemikalie, der får katte til at gå amokKattenip har en velkendt effekt på, dets berusende højder er forårsaget af nepetalactone, en type kemikalie kaldet terpen. Kredit:John Innes Center Forskere ved John Innes Center har kastet lys ov
Hvordan katteurt gør det kemikalie, der får katte til at gå amokKattenip har en velkendt effekt på, dets berusende højder er forårsaget af nepetalactone, en type kemikalie kaldet terpen. Kredit:John Innes Center Forskere ved John Innes Center har kastet lys ov -
 COF-999:Et porøst pulver, der fanger CO₂ direkte fra den omgivende luftYuji Sakai/Getty Images Menneskeskabt CO₂ er en førende drivkraft bag klimaændringer. Mens direkte luftopsamling historisk set har været rettet mod højkoncentrerede røggasser fra kraftværker, viser e
COF-999:Et porøst pulver, der fanger CO₂ direkte fra den omgivende luftYuji Sakai/Getty Images Menneskeskabt CO₂ er en førende drivkraft bag klimaændringer. Mens direkte luftopsamling historisk set har været rettet mod højkoncentrerede røggasser fra kraftværker, viser e -
 Kemikere opdager ny reaktivitet af anstrengte molekylerMünster-teamet bruger denne laboratorieopsætning til at udføre fotocykloaddition. Kredit:University of Münster - Roman Kleinmans I syntetisk organisk kemi er såkaldte cycloadditioner en særlig vigt
Kemikere opdager ny reaktivitet af anstrengte molekylerMünster-teamet bruger denne laboratorieopsætning til at udføre fotocykloaddition. Kredit:University of Münster - Roman Kleinmans I syntetisk organisk kemi er såkaldte cycloadditioner en særlig vigt -
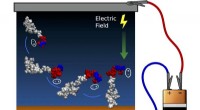 Implanterbart medicinsk udstyr forstærket af næste generations overflademodifikationKontrol af peptidorientering ved hjælp af elektrisk felt. Ladeseparation i den ene ende af peptidet skaber et dipolmoment (angivet med ellipser), der flugter med det elektriske felt og roterer hele mo
Implanterbart medicinsk udstyr forstærket af næste generations overflademodifikationKontrol af peptidorientering ved hjælp af elektrisk felt. Ladeseparation i den ene ende af peptidet skaber et dipolmoment (angivet med ellipser), der flugter med det elektriske felt og roterer hele mo
- Når en syre og alkali eller en basis neutraliserer hinanden, hvilket produkt dannes?
- Forskere advarer om, at moderne slaveri er blevet forværret af COVID-19
- Hvad er den sjældneste slags rock i verden?
- Hvilke to styrker antydede Alfred Wegener var ansvarlig for bevægelsen af kontinenter?
- "The Disadvantages of Copper Wire
- Hvilket svar forklarer bedst, hvorfor en fysiker ville studere den varme, der blev afgivet af Sun?


