Overgangsmetaller:Almindelige ionladninger og variable oxidationstilstande
* Variable oxidationstilstande: Overgangsmetaller har flere elektroner i deres d-orbitaler, som er involveret i binding. Dette giver dem mulighed for at miste forskellige antal elektroner, hvilket resulterer i forskellige oxidationstilstande (positive ladninger).
* Almindelige oxidationstilstande: Mens de kan have en række forskellige oxidationstilstande, er nogle mere almindelige end andre. For eksempel er almindelige oxidationstilstande for jern (Fe) +2 og +3, mens kobber (Cu) ofte har +1 og +2.
Vigtig bemærkning: Den specifikke ladning af en overgangsmetalion afhænger af grundstoffet og det kemiske miljø, det befinder sig i.
Lad mig vide, hvis du vil have eksempler på specifikke overgangsmetaller og deres almindelige ioner!
 Varme artikler
Varme artikler
-
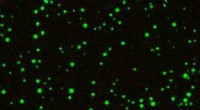 Forskere undersøger, hvordan forskellige flydende organeller i celler skabesSom stjerner i natten, flydende dråber af RNA (de lyse grønne kugler) flyder i en opløsning indeholdende høje koncentrationer af divalente magnesiumkationer. Dråberne afbildes gennem konfokal fluoresc
Forskere undersøger, hvordan forskellige flydende organeller i celler skabesSom stjerner i natten, flydende dråber af RNA (de lyse grønne kugler) flyder i en opløsning indeholdende høje koncentrationer af divalente magnesiumkationer. Dråberne afbildes gennem konfokal fluoresc -
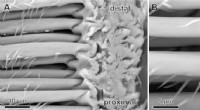 Overraskende opdagelse af edderkoppehår kan inspirere til stærkere klæbemidlerScanning Electron Microscopy (SEM) billede af baserne af pretarsal (dvs. på nederste del af benet) klæbende hår. (A) Til venstre er hårskaftene på de klæbende hår nærmest exoskeleton. Ved deres indsæt
Overraskende opdagelse af edderkoppehår kan inspirere til stærkere klæbemidlerScanning Electron Microscopy (SEM) billede af baserne af pretarsal (dvs. på nederste del af benet) klæbende hår. (A) Til venstre er hårskaftene på de klæbende hår nærmest exoskeleton. Ved deres indsæt -
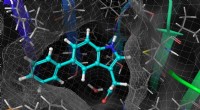 Lab-lavet hormon kan afsløre planters hemmelige livEn syntetisk version af auxin og dets proteinreceptor (lyseblå) lægger sig sammen, skabe et konstrueret par, der opfører sig ligesom det naturlige. Kredit:Keiko Torii/University of Washington/Howard H
Lab-lavet hormon kan afsløre planters hemmelige livEn syntetisk version af auxin og dets proteinreceptor (lyseblå) lægger sig sammen, skabe et konstrueret par, der opfører sig ligesom det naturlige. Kredit:Keiko Torii/University of Washington/Howard H -
 Team tager gætterierne ud af at opdage nye legeringer med høj entropiDette er et scanningelektronmikroskops tilbagespredende billede af legeringen Mo/W/Ta/Ti/Zr, med den lysere kontrast (Mo, W, Ta) -baseret fast løsning, mens den mørkere fase er (Ti, Zr) -rig fase. Kre
Team tager gætterierne ud af at opdage nye legeringer med høj entropiDette er et scanningelektronmikroskops tilbagespredende billede af legeringen Mo/W/Ta/Ti/Zr, med den lysere kontrast (Mo, W, Ta) -baseret fast løsning, mens den mørkere fase er (Ti, Zr) -rig fase. Kre
- Forskere afslører rollerne for vindstress og koldt vand under overfladen i det andet års afkøling…
- Bevægelsen mod ligestilling er bremset på nogle områder, gået i stå i andre, nye fem årtiers u…
- Gamle træringe tyder på, at solpletcyklusser har været i gang i 290 millioner år
- Hvad sker der, når zinksulfat reagerer med kaliumhydroxid?
- Hvad er forholdet mellem hastigheder lysstråler bølgelængder 4000 A og 8000A?
- Konvertering af et hvilket som helst tal til en procentdel:En praktisk vejledning med eksempler


