Faktorer, der påvirker hydrogenbindingsstyrken:Temperatur, opløsningsmiddel og pH
1. Temperatur: Når temperaturen stiger, får molekylerne mere kinetisk energi og vibrerer mere intenst. Denne øgede vibration forstyrrer de elektrostatiske interaktioner, der holder hydrogenbindingen sammen.
2. Opløsningsmiddel: Polære opløsningsmidler kan konkurrere med hydrogenbindingsinteraktionerne. For eksempel kan vandmolekyler danne brintbindinger med de molekyler, der tidligere var hydrogenbundet til hinanden, og dermed svække den oprindelige binding.
3. pH: Ekstreme pH-værdier kan forstyrre ladningsfordelingen af de molekyler, der er involveret i hydrogenbinding. For eksempel kan en lav pH (sur) protonere acceptormolekylet, hvilket svækker hydrogenbindingen. På samme måde kan en høj pH (basisk) deprotonere donormolekylet og opnå samme effekt.
4. Afstand: Styrken af en hydrogenbinding er omvendt proportional med afstanden mellem donor- og acceptoratomerne. Efterhånden som afstanden øges, svækkes de elektrostatiske vekselvirkninger.
5. Bindingsvinkel: Den optimale vinkel for en hydrogenbinding er lineær (180°). Afvigelser fra denne vinkel kan reducere styrken af bindingen.
6. Substituenter: Tilstedeværelsen af voluminøse substituenter nær hydrogenbindingsstedet kan skabe sterisk hindring, hvilket gør det vanskeligt for molekylerne at nærme sig hinanden og danne en stærk binding.
7. Elektrostatiske interaktioner: Tilstedeværelsen af andre stærke elektrostatiske interaktioner (som ionbindinger) kan konkurrere med hydrogenbindinger og svække dem.
8. Entropi: Dannelsen af en hydrogenbinding begrænser bevægelsesfriheden for de involverede molekyler, hvilket reducerer entropien. Dette fald i entropi gør dannelsen af hydrogenbindinger mindre gunstig, især ved højere temperaturer.
Det er vigtigt at huske, at disse faktorer er indbyrdes forbundne og ofte virker i kombination for at påvirke styrken af brintbindinger.
 Varme artikler
Varme artikler
-
 Her er et twist til en ældgammel klassiker:Laktosefri chokolademælkTo nordøstlige kandidater har bragt skifer, deres mærke af laktosefri chokolademælk, på hylderne i mere end 300 dagligvarebutikker langs østkysten. Kredit:Matthew Modoono/Northeastern University F
Her er et twist til en ældgammel klassiker:Laktosefri chokolademælkTo nordøstlige kandidater har bragt skifer, deres mærke af laktosefri chokolademælk, på hylderne i mere end 300 dagligvarebutikker langs østkysten. Kredit:Matthew Modoono/Northeastern University F -
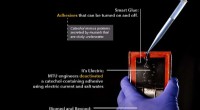 Ingeniører zapper og løsner smart undervandslimTænd og sluk for vedhæftning er det, der gør en lim smart. Det er én ting at gøre dette i det fri og noget helt andet under vand. Inspireret af naturen, katekoler er syntetiske forbindelser, der efter
Ingeniører zapper og løsner smart undervandslimTænd og sluk for vedhæftning er det, der gør en lim smart. Det er én ting at gøre dette i det fri og noget helt andet under vand. Inspireret af naturen, katekoler er syntetiske forbindelser, der efter -
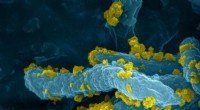 Skinner lys for at lave brintD. desulfuricans-CdS hybrider udviser høj H2 produktionsaktivitet, høj stabilitet og en bemærkelsesværdig effektivitet ved direkte brug af solenergi. Kredit:Inês Cardoso Pereira; Mónica Martins De
Skinner lys for at lave brintD. desulfuricans-CdS hybrider udviser høj H2 produktionsaktivitet, høj stabilitet og en bemærkelsesværdig effektivitet ved direkte brug af solenergi. Kredit:Inês Cardoso Pereira; Mónica Martins De -
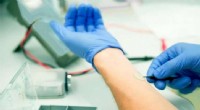 Blødt materiale inspireret af græshopper til bedre elektrodeklæbemiddelETH -forskere har udviklet en klæbende elektrode til sundhedsovervågning. En ny spin-off planlægger at bringe den på markedet i år. Kredit:ETH Zürich Forskere ved ETH Zürich har udviklet en ny typ
Blødt materiale inspireret af græshopper til bedre elektrodeklæbemiddelETH -forskere har udviklet en klæbende elektrode til sundhedsovervågning. En ny spin-off planlægger at bringe den på markedet i år. Kredit:ETH Zürich Forskere ved ETH Zürich har udviklet en ny typ
- Hvad var den romantiske holdning til videnskab?
- Hvad laver planter for at gengive noget?
- Hvorfor morgenfruer er et must at tilføje:Den skjulte skadedyrsbekæmpelseskraft i din have
- Hvad er membranen af græs?
- Dollars og dufte:Hvordan de rigtige lugte kan tilskynde kunder til at købe sundere fødevarer
- En ny måde at skabe molekyler til lægemiddeludvikling


