Forståelse af faseændringer:Et molekylært perspektiv
Her er en oversigt over, hvad der sker på molekylært niveau:
Energi- og faseændringer:
* Energi absorberes: Under faseændringer som smeltning, kogning eller sublimering absorberer stoffet energi. Denne energi bruges til at overvinde de intermolekylære kræfter, der holder molekylerne sammen i den foregående fase.
* Energi frigives: Under faseændringer som frysning, kondensation eller aflejring frigiver stoffet energi. Denne energi frigives efterhånden som molekylerne mister energi og danner stærkere bindinger, der går over i en mere ordnet tilstand.
Nøglekarakteristika:
* Temperaturen forbliver konstant: Under et faseskift forbliver stoffets temperatur konstant på trods af tilførsel eller fjernelse af varme. Dette skyldes, at energien bliver brugt til at bryde eller danne bindinger i stedet for at hæve molekylernes kinetiske energi.
* Ændring i molekylært arrangement: Molekylerne i et stof har forskellige arrangementer afhængigt af deres fase. For eksempel i et fast stof er molekyler tæt pakket og har et fast arrangement. I en væske er molekyler mere løst pakket og kan bevæge sig rundt. I en gas er molekyler langt fra hinanden og bevæger sig frit.
Eksempler på faseændringer:
* Smeltning: Is (fast) til vand (flydende)
* Fryser: Vand (flydende) til is (fast)
* Kogning: Vand (væske) til damp (gas)
* Kondensering: Damp (gas) til vand (væske)
* Sublimering: Tøris (fast) til kuldioxid (gas)
* Deponering: Kuldioxid (gas) til tøris (fast)
Anvendelser af faseændringer:
Faseændringer er afgørende i mange naturlige processer og industrielle anvendelser:
* Vejret: Kondens danner skyer, og fordampning driver vandets kredsløb.
* Køling: Fordampningen af kølemidler i køleskabe absorberer varme og afkøler indersiden.
* Industrielle processer: Faseændringer bruges i destillation, krystallisation og andre separationsprocesser.
Sammenfattende involverer faseændringer ændringer i et stofs molekylære arrangement og energitilstand, hvilket resulterer i en overgang mellem forskellige stoftilstande.
 Varme artikler
Varme artikler
-
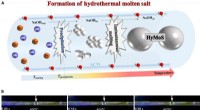 Et nyt opløsningsmiddelsystem:Hydrotermalt smeltet saltDannelse af HyMoS. (A) Skema for dannelsen af HyMoS i SCW, med eksemplet på NaOH. (B) Montagebillede fra film S1 (nedenfor), der viser den direkte observation og bevægelse af en smeltet NaOH -dråbe
Et nyt opløsningsmiddelsystem:Hydrotermalt smeltet saltDannelse af HyMoS. (A) Skema for dannelsen af HyMoS i SCW, med eksemplet på NaOH. (B) Montagebillede fra film S1 (nedenfor), der viser den direkte observation og bevægelse af en smeltet NaOH -dråbe -
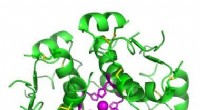 Forskere bruger zink til at målrette insulinproducerende celler med regenerativ medicinHøjopløsningsmodel af seks insulinmolekyler samlet i en hexamer. Kredit:Isaac Yonemoto/Wikipedia En insulininjektion kan håndtere diabetessymptomer, men faktisk at helbrede sygdommen ville betyde
Forskere bruger zink til at målrette insulinproducerende celler med regenerativ medicinHøjopløsningsmodel af seks insulinmolekyler samlet i en hexamer. Kredit:Isaac Yonemoto/Wikipedia En insulininjektion kan håndtere diabetessymptomer, men faktisk at helbrede sygdommen ville betyde -
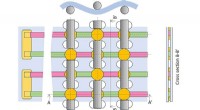 Kropsvarme gennem fleksibelt stof kunne drive IoT-enheder til sundhedsovervågning for mennesker, kæ…Forskere ved Purdue University har skabt en teknologi til at løse tykkelsesproblemet for bærbar strømproduktion. Kredit:Purdue University Bærbar elektronik og andre Internet of Things (IoT) enhede
Kropsvarme gennem fleksibelt stof kunne drive IoT-enheder til sundhedsovervågning for mennesker, kæ…Forskere ved Purdue University har skabt en teknologi til at løse tykkelsesproblemet for bærbar strømproduktion. Kredit:Purdue University Bærbar elektronik og andre Internet of Things (IoT) enhede -
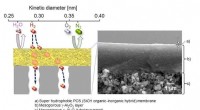 Ny brintbrændstofrensningsmembran baner vejen for en grønnere fremtidEt tværsnitsbillede af selektiv hydrogengennemtrængning i en superhydrofob membran dannet på en porøs rørformet understøtning. Kredit:Yuji Iwamoto fra Nagoya Institute of Technology Brint er bleve
Ny brintbrændstofrensningsmembran baner vejen for en grønnere fremtidEt tværsnitsbillede af selektiv hydrogengennemtrængning i en superhydrofob membran dannet på en porøs rørformet understøtning. Kredit:Yuji Iwamoto fra Nagoya Institute of Technology Brint er bleve
- Ny fare for koraller i opvarmende have:Metalforurening
- Hvad sker der, når en solid frigiver energi?
- RNA er til dig som DNA til?
- Hvorfor er en madweb mere nøjagtig end kæde ved at beskrive, hvordan energi overført gennem et ø…
- Hvordan ser en meteor ud, når den striber over nattehimlen?
- Generationen af en plante, der er ansvarlig for at producere gameter, er?


