Kobber(I)sulfid (Cu₂S) elektronpunktdiagram:en trin-for-trin guide
Forstå komponenterne
* Kobber (I): Kobber i sin +1 oxidationstilstand har en enkelt valenselektron.
* Svovl: Svovl har seks valenselektroner.
Tegning af diagrammet
1. Start med svovl: Tegn symbolet "S" og placer seks prikker omkring det for at repræsentere dets valenselektroner. De skal arrangeres sådan:
```
..
:S:
..
```
2. Tilføj kobberatomerne: Tegn to kobberatomer ("Cu") ved siden af svovlen, hver med en prik, der repræsenterer dens valenselektron.
```
...
:S:Cu Cu
...
```
3. Udfør obligationer: Svovl har brug for to elektroner mere for at fuldføre sin oktet. Hvert kobberatom deler sin enkelte elektron med svovl og danner en kovalent binding.
```
...
:S:.Cu. Cu
...
```
Vigtige bemærkninger
* Dette elektronprikdiagram er en forenklet repræsentation. Den faktiske binding i Cu₂S er mere kompleks og involverer metallisk og kovalent binding.
* Elektronprikdiagrammer bruges primært til at illustrere valenselektronens involvering i binding, ikke den præcise molekylære struktur.
Lad mig vide, hvis du har andre anmodninger om elektronprikdiagram!
Sidste artikelIoniske forbindelser med fluor:Hvilke elementer danner dem?
Næste artikelKemisk formel:Forstå elementsammensætning og forhold
 Varme artikler
Varme artikler
-
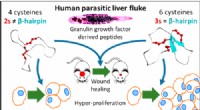 Et molekyle produceret af en thailandsk leverparasit kan være løsningen på de ikke-helende sårKredit:ACS Hver dag amputeres 12 australske diabetikere på grund af et sår, der ikke heler. Globalt set det er en hvert 30. sekund. Et molekyle produceret af en thailandsk leverparasit kan være l
Et molekyle produceret af en thailandsk leverparasit kan være løsningen på de ikke-helende sårKredit:ACS Hver dag amputeres 12 australske diabetikere på grund af et sår, der ikke heler. Globalt set det er en hvert 30. sekund. Et molekyle produceret af en thailandsk leverparasit kan være l -
 Udvikling af ledende og elektrokatalytiske mediatorer i Li-S-batterierFe-MoSe2 @rGO giver en lovende mulighed for at producere en udviklet separatorfunktion til praktiske Li-S-batterier med høj energidensitet. Fe-MoSe2 @rGO-PP udviser fremragende cykelstabilitet under m
Udvikling af ledende og elektrokatalytiske mediatorer i Li-S-batterierFe-MoSe2 @rGO giver en lovende mulighed for at producere en udviklet separatorfunktion til praktiske Li-S-batterier med høj energidensitet. Fe-MoSe2 @rGO-PP udviser fremragende cykelstabilitet under m -
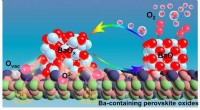 Mekanisme for oxygenaktivering på bariumholdige perovskitmaterialerOxygenaktiveringsmekanisme på Ba-holdige perovskitoxider. Kredit:Zhu Yue Et forskerhold ledet af prof. Yang Weishen og prof. Zhu Xuefeng fra Dalian Institute of Chemical Physics (DICP) fra det kine
Mekanisme for oxygenaktivering på bariumholdige perovskitmaterialerOxygenaktiveringsmekanisme på Ba-holdige perovskitoxider. Kredit:Zhu Yue Et forskerhold ledet af prof. Yang Weishen og prof. Zhu Xuefeng fra Dalian Institute of Chemical Physics (DICP) fra det kine -
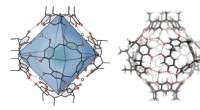 Ny tilgang til terpensynteserTil venstre, det omkring 1,4 kubik nanometer store hulrum i den molekylære kapsel er fremhævet med blåt. Til højre, samhørigheden af kapslen via hydrogenbindinger (grønne stiplede linjer) er synlig.
Ny tilgang til terpensynteserTil venstre, det omkring 1,4 kubik nanometer store hulrum i den molekylære kapsel er fremhævet med blåt. Til højre, samhørigheden af kapslen via hydrogenbindinger (grønne stiplede linjer) er synlig.
- Ornitologer opdager, at verdens største kolibri faktisk er to arter
- Selvstændig erhvervsdrivende blandt hårdest ramt af pandemi
- Magma, der er sprængt i luften og hærder er?
- Tror du, at al din plastik bliver genbrugt? Ny forskning viser, at den kan ende i havet
- Hvad er resultater i videnskab?
- Hvad er Campyla Bacter?


