Forståelse af oxidationstal for overgangsmetaller:En trin-for-trin guide
1. Regler at huske:
* Gratis elementer: Oxidationstallet for et grundstof i dets grundstofform er altid 0.
* Monatomiske ioner: Oxidationstallet for en monoatomisk ion er lig med dens ladning. For eksempel Fe 2+ har et oxidationstal på +2.
* Oxygen: Oxygen har normalt et oxidationstal på -2, undtagen i peroxider (hvor det er -1) og i forbindelser med fluor (hvor det er positivt).
* Brint: Brint har normalt et oxidationstal på +1, undtagen i metalhydrider, hvor det er -1.
* Summen af oxidationstal: I en neutral forbindelse skal summen af oxidationstal for alle atomer være lig med nul. I en polyatomisk ion skal summen af oxidationstal svare til ladningen af ionen.
2. Strategier for overgangselementer:
* Kendte oxidationstilstande: Nogle overgangselementer har fælles oxidationstilstande. f.eks.
* Chrom har ofte +2, +3 og +6 oxidationstilstande.
* Mangan har almindeligvis +2, +4, +6 og +7 oxidationstilstande.
* Jern er normalt +2 eller +3.
* Brug de andre elementer: Hvis du kender oxidationstallene for de andre grundstoffer i forbindelsen, kan du udlede overgangselementets oxidationstal. For eksempel i KMnO4 :
* Kalium (K) har en +1 oxidationstilstand.
* Ilt (O) har en -2 oxidationstilstand.
* For at balancere ladningerne skal mangan (Mn) have en +7 oxidationstilstand:(+1) + (+7) + 4(-2) =0
* Anioniske ligander: Når overgangselementer danner komplekser med anioniske ligander (som Cl-, CN-), beregnes metallets oxidationstilstand ved at trække den samlede negative ladning fra kompleksets samlede ladning. For eksempel i [Fe(CN)6 ] 4- :
* Cyanid (CN-) har en ladning -1.
* Den samlede afgift for komplekset er -4.
* Oxidationstilstanden for jern (Fe) beregnes som +2:-4 - (6 x -1) =+2
3. Eksempler:
* FeCl3 : Klor (Cl) har et oxidationstal på -1. For at balancere skal jern (Fe) have en +3 oxidationstilstand:(+3) + 3(-1) =0
* Cr2 O7 2- : Ilt (O) har et oxidationstal på -2. Den samlede ladning af dichromationen er -2. For at balancere skal chrom (Cr) have en +6 oxidationstilstand:2(+6) + 7(-2) =-2
* [Co(NH3 )6 ]Cl3 : Ammoniak (NH3 ) er neutral. Chlorid (Cl) har et oxidationstal på -1. For at balancere skal kobolt (Co) have en +3 oxidationstilstand:(+3) + 3(-1) =0
Vigtige bemærkninger:
* Variable oxidationstilstande: Mange overgangselementer udviser flere oxidationstilstande, så oxidationstallet kan variere afhængigt af den specifikke forbindelse.
* Ikke altid heltalværdier: I nogle tilfælde er oxidationstallet for et overgangselement muligvis ikke et heltal.
* Formel debitering: Oxidationstal er et formelt ladningssystem og repræsenterer ikke nødvendigvis den sande fordeling af elektroner i et molekyle.
Lad mig vide, hvis du har nogle specifikke eksempler, du vil arbejde igennem!
 Varme artikler
Varme artikler
-
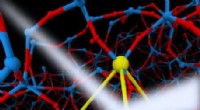 Hvad forårsager den top? Besvarelse af et langvarigt spørgsmål om kovalente væskerRøntgenspredning (hvid beem) billede af lokal tetraedrisk orden dannet af Si-atomer (store gule partikler) i flydende silica (Si-atomer er store partikler og O-atomer er små partikler) ved simulering.
Hvad forårsager den top? Besvarelse af et langvarigt spørgsmål om kovalente væskerRøntgenspredning (hvid beem) billede af lokal tetraedrisk orden dannet af Si-atomer (store gule partikler) i flydende silica (Si-atomer er store partikler og O-atomer er små partikler) ved simulering. -
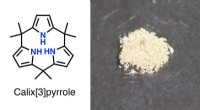 Pyrrolkemi:Gode ting kommer i treDen kemiske struktur og faststofkrystaller af calix[3]pyrrol. Kredit:Inokuma Laboratory En ny tilgang fører til den længe ventede dannelse af ringe lavet af tre pyrroler, som kunne bruges til at f
Pyrrolkemi:Gode ting kommer i treDen kemiske struktur og faststofkrystaller af calix[3]pyrrol. Kredit:Inokuma Laboratory En ny tilgang fører til den længe ventede dannelse af ringe lavet af tre pyrroler, som kunne bruges til at f -
 Mestring af molforhold:Fra empiriske formler til afbalancerede ligningerAf Chris Deziel | Opdateret 24. marts 2022 Inden for støkiometriens område - hvor kemikere sammenligner de relative mængder af stoffer i reaktioner - er det vigtigt at vide, hvordan man bestemmer mol
Mestring af molforhold:Fra empiriske formler til afbalancerede ligningerAf Chris Deziel | Opdateret 24. marts 2022 Inden for støkiometriens område - hvor kemikere sammenligner de relative mængder af stoffer i reaktioner - er det vigtigt at vide, hvordan man bestemmer mol -
 Mikrofluidiske enheder afklarer, hvordan dispergeringsmidler modificerer asfalten for at holde rør …Ris postdoc-forsker Peng He, venstre, og kandidatstuderende Yu-Jiun Lin kører en prøve af råolie gennem en mikrofluidisk enhed, der giver dem mulighed for at se opbygningen af asfaltener i realtid.
Mikrofluidiske enheder afklarer, hvordan dispergeringsmidler modificerer asfalten for at holde rør …Ris postdoc-forsker Peng He, venstre, og kandidatstuderende Yu-Jiun Lin kører en prøve af råolie gennem en mikrofluidisk enhed, der giver dem mulighed for at se opbygningen af asfaltener i realtid.
- Hvilke to former for energi kunne bedst bruges til at øge temperaturen et ark kobber?
- Hvilken type stenformer på grund af opvarmning og afkøling?
- Hvordan ved forskere, hvad solen er lavet af i atmosfæren?
- Hvordan måles gas i?
- Hvad er sjette største planet i solsystemet?
- Hvad er energikilden for alle økologiske pyramider?


