Mestring af molforhold:Fra empiriske formler til afbalancerede ligninger
Af Chris Deziel | Opdateret 24. marts 2022
Inden for støkiometriens område - hvor kemikere sammenligner de relative mængder af stoffer i reaktioner - er det vigtigt at vide, hvordan man bestemmer molforholdet. Uanset om du udarbejder den empiriske formel for en ukendt forbindelse eller beregner de præcise mængder af reaktanter og produkter i en reaktion, er principperne de samme:identificer det enkleste heltalsforhold mellem de involverede arter.
Beslutning af en empirisk formel
Når en mystisk forbindelse analyseres for dens grundstofsammensætning, vil du normalt måle massen af hvert tilstedeværende element. Konvertering af disse masser til mol (masse ÷ atomvægt) afslører, hvor mange mol af hvert grundstof der findes. Derfra kan du udlede det enkleste hele-talsforhold – den empiriske formel.
- Beregn mol af hvert grundstof. Divider den målte masse med grundstoffets atomvægt. For eksempel giver en forbindelse, der indeholder 0,675 g H, 10,8 g O og 13,5 g Ca:
- H:0,675 g ÷ 1,01 gmol⁻¹ =0,675 mol
- O:10,8 g ÷ 16,00 gmol⁻¹ =0,675 mol
- Ca:13,5 g ÷ 40,08 gmol⁻¹ =0,337 mol
- Divider med den mindste molværdi. Her er Ca (0,337 mol) den mindste. At dividere hver molværdi med 0,337 giver:
- H:0,675 ÷ 0,337 ≈ 2
- O:0,675 ÷ 0,337 ≈ 2
- Ca:0,337 ÷ 0,337 =1
- Skriv den empiriske formel. De resulterende heltalsforhold bliver sænkede:CaO₂H₂, typisk udtrykt som Ca(OH)₂.
Afbalancering af en reaktionsligning
Når reaktanterne og produkterne af en reaktion er kendt, kan du skrive en ubalanceret ligning og derefter afbalancere den ved at justere støkiometriske koefficienter. Disse koefficienter er faktisk de molforhold, der opfylder loven om bevarelse af masse.
- Start med den ubalancerede ligning. For eksempel:H2 + O2 → H2O.
- Balancer atomerne. Multiplicer hver side med det mindste sæt af heltal, der udligner antallet af atomer for hvert element. Den afbalancerede ligning bliver:2H₂ + O₂ → 2H₂O.
- Fortolk molforholdene. Fra koefficienterne:
- Brint til oxygen:2molH₂ :1molO₂ → 2:1
- Oxygen til vand:1molO₂ :2molH₂O → 1:2
- Vand til brint:2molH₂O :4molH₂ → 1:2 (forenklet)
Disse koefficienter afbalancerer ikke kun ligningen, men fortæller dig også, hvor mange mol af hver art, der deltager i reaktionen. At beherske denne teknik sikrer nøjagtige støkiometriske beregninger for enhver kemisk proces.
 Varme artikler
Varme artikler
-
 Membranløse protoceller kunne give spor til dannelsen af tidligt livMembranløse protoceller - kaldet komplekse koacervater - kan samle RNA-molekyler, hvilket gør det muligt for RNAerne at udføre visse reaktioner, et vigtigt skridt i livets oprindelse på Jorden. Billed
Membranløse protoceller kunne give spor til dannelsen af tidligt livMembranløse protoceller - kaldet komplekse koacervater - kan samle RNA-molekyler, hvilket gør det muligt for RNAerne at udføre visse reaktioner, et vigtigt skridt i livets oprindelse på Jorden. Billed -
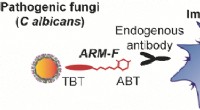 Neutralisering af patogene svampe med småmolekylære immunterapeutikaKredit:Wiley Svampeinfektioner repræsenterer en stigende sundhedskrise, især for immundefekt patienter. Amerikanske forskere rapporterer nu i tidsskriftet Angewandte Chemie at specifik hjælp kun
Neutralisering af patogene svampe med småmolekylære immunterapeutikaKredit:Wiley Svampeinfektioner repræsenterer en stigende sundhedskrise, især for immundefekt patienter. Amerikanske forskere rapporterer nu i tidsskriftet Angewandte Chemie at specifik hjælp kun -
 Forskere finder molekylær ødelæggelseskode for enzym involveret i kolesterolproduktionUNSW ph.d.-kandidat Jake Chua er hovedforfatter på et papir, der viser, hvordan et nøgleenzym, der bidrager til kolesterolproduktion, kan reguleres - og ødelægges - ved hjælp af et bestemt molekyle. K
Forskere finder molekylær ødelæggelseskode for enzym involveret i kolesterolproduktionUNSW ph.d.-kandidat Jake Chua er hovedforfatter på et papir, der viser, hvordan et nøgleenzym, der bidrager til kolesterolproduktion, kan reguleres - og ødelægges - ved hjælp af et bestemt molekyle. K -
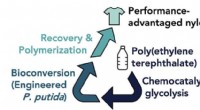 Forskere konstruerer mikroorganismer til at tackle PET-plastikforureningNREL- og ORNL-forskere har udviklet en metode til at opgradere PET til præstationsfordelagtig nylon, en forløber for andre værdifulde produkter såsom vandtæt tøj, stiftfri belægning af køkkengrej, og
Forskere konstruerer mikroorganismer til at tackle PET-plastikforureningNREL- og ORNL-forskere har udviklet en metode til at opgradere PET til præstationsfordelagtig nylon, en forløber for andre værdifulde produkter såsom vandtæt tøj, stiftfri belægning af køkkengrej, og


