Grafit vs. Diamant:Delte kulstofallotroper og deres fælles egenskaber
Af Michael E Carpenter | Opdateret 24. marts 2022
Forskellene mellem diamanter og grafit er slående i udseende, hårdhed og typiske anvendelser. Men når de undersøges på atomniveau, afslører de to materialer et bemærkelsesværdigt sæt fælles egenskaber.
Kulstof
Både grafit og diamanter er sammensat af rene kulstofatomer. Denne fælles kemiske sammensætning gør dem til allotroper - forskellige strukturelle former af det samme element - sammen med amorft kulstof (sod eller kønrøg). Forskellen ligger i, hvordan hvert kulstofatom binder sig til dets naboer, hvilket producerer divergerende fysiske egenskaber.
Kovalente bindinger
I begge allotroper er carbonatomerne forbundet med stærke kovalente bindinger, der deler valenselektroner. Disse bindinger udgør rygraden i hvert materiales struktur, hvilket dikterer styrke, ledningsevne og reaktivitet.
Høje smeltepunkter
Grafit smelter med ekstraordinære 4.200 K, mens diamant smelter ved 4.500 K. Under ekstrem varme og ionbombardement kan diamant omdannes tilbage til grafit, den mere termodynamisk stabile form for kulstof under disse forhold.
Naturligt forekommende
Både grafit og diamanter forekommer naturligt på Jorden, selvom de også kan syntetiseres i laboratorier. I modsætning til deres naturlige modstykker har hvidt kulstof – en laboratorieskabt form, der kan opdele en lysstråle i to – ingen naturlig analog.
Disse fællestræk understreger, hvorfor begge materialer er værdsat inden for forskellige områder, fra skærende værktøjer til elektronik, på trods af deres tilsyneladende forskelle.
 Varme artikler
Varme artikler
-
 Gør en almindelig plast til molekyler af høj værdiEn simpel one-pot proces gør polyethylenplastaffald til værdifulde væsker, når det udsættes for en fast kemisk katalysator og lidt varme. Kredit:Fan Zhang, UCSB, CC BY-SA Hvis du troede, at de spi
Gør en almindelig plast til molekyler af høj værdiEn simpel one-pot proces gør polyethylenplastaffald til værdifulde væsker, når det udsættes for en fast kemisk katalysator og lidt varme. Kredit:Fan Zhang, UCSB, CC BY-SA Hvis du troede, at de spi -
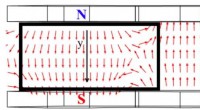 Magnetfelters indflydelse på tyndfilmstrukturerVisualisering af et magnetfelt mellem permanente magneter ved placeringen af substratet til aflejring af NiFe/IrMn film tyndfilmstruktur. Kredit:Valeria Rodionova Et team af forskere fra Immanue
Magnetfelters indflydelse på tyndfilmstrukturerVisualisering af et magnetfelt mellem permanente magneter ved placeringen af substratet til aflejring af NiFe/IrMn film tyndfilmstruktur. Kredit:Valeria Rodionova Et team af forskere fra Immanue -
 Discovery booster teorien om, at liv på Jorden opstod fra RNA-DNA-blandingKredit:CC0 Public Domain Kemikere ved Scripps Research har gjort en opdagelse, der understøtter et overraskende nyt syn på, hvordan liv opstod på vores planet. I en undersøgelse offentliggjort i
Discovery booster teorien om, at liv på Jorden opstod fra RNA-DNA-blandingKredit:CC0 Public Domain Kemikere ved Scripps Research har gjort en opdagelse, der understøtter et overraskende nyt syn på, hvordan liv opstod på vores planet. I en undersøgelse offentliggjort i -
 Nyt center til at erstatte olie og gas med bæredygtig kemiKredit:Københavns Universitet Mange af de ting, der omgiver os, er kemisk afledt af fossil gas og olie - fra vaskepulver til telefoner til lægemidler. Som sådan, kemi bidrager til CO 2 emissione
Nyt center til at erstatte olie og gas med bæredygtig kemiKredit:Københavns Universitet Mange af de ting, der omgiver os, er kemisk afledt af fossil gas og olie - fra vaskepulver til telefoner til lægemidler. Som sådan, kemi bidrager til CO 2 emissione
- Hvordan blander du redken chromatics?
- 2 steder på jorden, hvor organiske molekyler kunne have været syntetiseret?
- Hvor mange satellitter har Jupiter og Saturn?
- Antag, at et objekt i frit fald falder fra en bygning af sin starthastighed 0 ignorerer virkningerne…
- Veg nudge:En ekstra vegetarisk mulighed reducerer kødforbruget uden at bule madsalget
- Senvinterstorme letter Californiens dyk tilbage i tørken


