Natriumbicarbonat og eddikesyrereaktion:kemi forklaret
* Natriumethanoat (CH₃COONa)
* Carbondioxid (CO₂) gas
* Vand (H₂O)
Her er den afbalancerede kemiske ligning:
NaHCO₃(aq) + CH3COOH(aq) → CH3COONa(aq) + CO₂(g) + H2O(l)
Forklaring:
* Etansyre (CH₃COOH) er en svag syre, der donerer en proton (H⁺).
* Natriumhydrogencarbonat (NaHCO₃) fungerer som en base, der accepterer protonen.
* Protonoverførslen danner natriumethanoat (CH₃COONa) , som er et salt.
* De resterende brint- og carbonationer kombineres og danner kuldioxidgas (CO₂) og vand (H2O) .
Observationer:
* Du vil observere bobler efterhånden som kuldioxidgas frigives.
* Reaktionen er exoterm , hvilket betyder, at den afgiver varme, og du kan mærke, at beholderen varmes op.
* Opløsningen bliver mindre sur, når ethansyren forbruges.
Denne reaktion bruges også i bagning til at producere kuldioxidgas, som hjælper brød og kager med at hæve. Det bruges også i nogle antacida til at neutralisere mavesyre.
 Varme artikler
Varme artikler
-
 Hvem vil nu gå videre med at validere retsvidenskabelige discipliner?Videnskaben og domstolene kan vægte tingene forskelligt. Kredit:Michael Coghlan, CC BY-SA Videnskab og jura er ikke naturlige partnere. Videnskaben søger at fremme vores forståelse af den naturlig
Hvem vil nu gå videre med at validere retsvidenskabelige discipliner?Videnskaben og domstolene kan vægte tingene forskelligt. Kredit:Michael Coghlan, CC BY-SA Videnskab og jura er ikke naturlige partnere. Videnskaben søger at fremme vores forståelse af den naturlig -
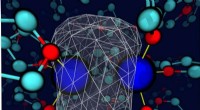 Kemikalier kan ændre deres identitet, takket være væskerne, hvor de opholder sigEt øjebliksbillede afslører, at det omgivende tetrahydrofuranopløsningsmiddel deformerer bindingselektrondensiteten omkring et opløst natrium. Natriumkernerne er blå kugler; valenselektronernes tæthed
Kemikalier kan ændre deres identitet, takket være væskerne, hvor de opholder sigEt øjebliksbillede afslører, at det omgivende tetrahydrofuranopløsningsmiddel deformerer bindingselektrondensiteten omkring et opløst natrium. Natriumkernerne er blå kugler; valenselektronernes tæthed -
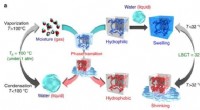 Forskere rapporterer om en temperaturfølsom gel, der absorberer og frigiver fugtIllustration af hovedbegreberne beskrevet i dette papir. Kredit:Kansai University Takashi Miyata ved Kansai University og kolleger melder ind Naturkommunikation en temperaturfølsom gel, der abso
Forskere rapporterer om en temperaturfølsom gel, der absorberer og frigiver fugtIllustration af hovedbegreberne beskrevet i dette papir. Kredit:Kansai University Takashi Miyata ved Kansai University og kolleger melder ind Naturkommunikation en temperaturfølsom gel, der abso -
 Moderne porøst materiale ligner XIV Century Alhambra mosaikKredit:Imdea Forskere fra Spanien og USA har syntetiseret en hidtil uset metal-organisk ramme (MOF), der indeholder en perfekt lineær brokæde, der viser en smuk lighed med en islamisk mosaik fra d
Moderne porøst materiale ligner XIV Century Alhambra mosaikKredit:Imdea Forskere fra Spanien og USA har syntetiseret en hidtil uset metal-organisk ramme (MOF), der indeholder en perfekt lineær brokæde, der viser en smuk lighed med en islamisk mosaik fra d


