Methanol vs. Methanthiol:Forstå kogepunktsforskelle
* Brintbinding i methanol (CH3OH): Methanol har et hydrogenatom bundet til et oxygenatom (O-H). Dette giver mulighed for hydrogenbinding, en stærk intermolekylær kraft, der opstår fra tiltrækningen mellem et delvist positivt hydrogenatom og et delvist negativt iltatom på tilstødende molekyler.
* Dipol-dipol-interaktioner i methanthiol (CH3SH): Methanthiol har et svovlatom bundet til et hydrogenatom (S-H). Mens S-H-bindingen er polær, er den mindre polær end O-H-bindingen i methanol. Derfor oplever methanthiol svagere dipol-dipol-interaktioner.
* London Dispersion Forces: Både methanol og methanthiol oplever London-spredningskræfter, som er svage intermolekylære kræfter, der opstår som følge af midlertidige udsving i elektronfordelingen. Imidlertid er disse kræfter generelt svagere end hydrogenbinding eller dipol-dipol-interaktioner.
Opsummering: Methanols stærke hydrogenbindingsinteraktioner er betydeligt stærkere end de svagere dipol-dipol-interaktioner i methanthiol. Disse stærkere intermolekylære kræfter i methanol kræver mere energi at overvinde, hvilket resulterer i et højere kogepunkt.
Sidste artikelIsotoper:At forstå atomer med det samme antal protoner
Næste artikelLithiumchlorid (LiCl):Formel, egenskaber og dannelse
 Varme artikler
Varme artikler
-
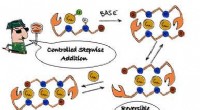 Bygning af molekylære ledninger, et atom ad gangenEn tegneserie af Dr. Rivada-Wheelaghan viser den enkle trinvise proces med kobberatomkædesyntese ved hjælp af en dynamisk ligand. Kobberatomer kan tilføjes eller fjernes en efter en for at lave kæder
Bygning af molekylære ledninger, et atom ad gangenEn tegneserie af Dr. Rivada-Wheelaghan viser den enkle trinvise proces med kobberatomkædesyntese ved hjælp af en dynamisk ligand. Kobberatomer kan tilføjes eller fjernes en efter en for at lave kæder -
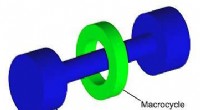 Forskere laver verdens hurtigste molekylære skytteSkematisk fremstilling af en rotaxan, den type molekyle, der var genstand for undersøgelsen. Kredit:Wikimedia Commons Takket være et smart kemisk design, Det er lykkedes forskere ved universitetet
Forskere laver verdens hurtigste molekylære skytteSkematisk fremstilling af en rotaxan, den type molekyle, der var genstand for undersøgelsen. Kredit:Wikimedia Commons Takket være et smart kemisk design, Det er lykkedes forskere ved universitetet -
 Ny interaktion mellem tyndfilmsmagneter til hurtigere hukommelsesenhederDr. Dong-Soo Han. Kredit:Eindhoven University of Technology Banebrydende opdagelse inden for elektromagnetisme åbner op for design af tredimensionelle spinstrukturer, som kunne være grundenhederne
Ny interaktion mellem tyndfilmsmagneter til hurtigere hukommelsesenhederDr. Dong-Soo Han. Kredit:Eindhoven University of Technology Banebrydende opdagelse inden for elektromagnetisme åbner op for design af tredimensionelle spinstrukturer, som kunne være grundenhederne -
 Hvordan bufferløsninger beskytter pH i forskning, biologi og industriAf Ethan Gallagher, Opdateret 30. august 2022 Buffernes rolle Bufferløsninger er uundværlige reagenser på tværs af kemi, biologi og industri. Deres primære fordel er deres evne til at modstå pH-skift
Hvordan bufferløsninger beskytter pH i forskning, biologi og industriAf Ethan Gallagher, Opdateret 30. august 2022 Buffernes rolle Bufferløsninger er uundværlige reagenser på tværs af kemi, biologi og industri. Deres primære fordel er deres evne til at modstå pH-skift


