Hvordan bufferløsninger beskytter pH i forskning, biologi og industri
Af Ethan Gallagher, Opdateret 30. august 2022
Buffernes rolle
Bufferløsninger er uundværlige reagenser på tværs af kemi, biologi og industri. Deres primære fordel er deres evne til at modstå pH-skift, hvilket sikrer, at reaktioner forløber under optimale forhold. I kemi påvirker pH - målet for en opløsnings surhedsgrad - direkte reaktionshastigheder og produktudbytte. Ved at opretholde en stabil pH-værdi muliggør buffere præcis kontrol over eksperimentelle resultater.
Syrer, konjugatbaser og buffersammensætning
Typiske buffere består af en svag syre og dens konjugerede base. Syrer donerer hydrogenioner (H⁺), hvilket øger surhedsgraden, mens baser accepterer H⁺ og reducerer det. Når en syre frigiver H⁺, bliver den resterende art dens konjugerede base. For eksempel dissocierer eddikesyre (CH3COOH) for at danne acetat (CH3COO⁻) og H+. Acetat-ionen kan derefter rekombinere med H⁺ for at omdanne eddikesyre, hvilket illustrerer den dynamiske ligevægt, der understøtter buffervirkning.
LeChateliers princip i bufferhandling
Fordi syre-base ligevægte er reversible, gælder LeChateliers princip. Tilsætning af ekstra H⁺ skubber ligevægten mod syreformen, indtager H⁺ og stabiliserer pH. På samme måde bruger indføring af en base H⁺, hvilket flytter ligevægten tilbage mod den konjugerede base. Denne selvregulerende adfærd gør det muligt for buffere at absorbere forstyrrelser fra syrer eller baser tilsat systemet.
Praktiske applikationer
Buffere er kritiske i biologien, hvor de opretholder blodets pH mellem 7,35 og 7,45 og muliggør enzymkatalyserede reaktioner, der kræver stram pH-kontrol. I laboratorieforskning er en specifik pH ofte afgørende for eksperimenter, der involverer proteiner, nukleinsyrer eller andre biomolekyler. Industrielt anvendes buffere i fermenteringsprocesser, farvestoffremstilling og farmaceutisk produktion for at sikre ensartet produktkvalitet og sikkerhed.
 Varme artikler
Varme artikler
-
 Laserbehandling viser potentiale for at reducere industriel kemisk behandling af køretøjerORNL-forsker Adrian Sabau beskriver komponenter i et laserinterferensstruktureringssystem, der blev brugt til at behandle aluminiumslegeringsplader til korrosionsbeskyttelse. Kredit:Carlos Jones/ORNL,
Laserbehandling viser potentiale for at reducere industriel kemisk behandling af køretøjerORNL-forsker Adrian Sabau beskriver komponenter i et laserinterferensstruktureringssystem, der blev brugt til at behandle aluminiumslegeringsplader til korrosionsbeskyttelse. Kredit:Carlos Jones/ORNL, -
 Forskere opnåede nye forbindelser med potentiel antitumoreffekt fra havsvampDen store del af forskningen relateret til syntese af målforbindelser blev udført af Polina Smirnova - en ph.d. studerende ved Institut for organisk kemi i SNS FEFU. Kredit:FEFUs pressekontor Kemi
Forskere opnåede nye forbindelser med potentiel antitumoreffekt fra havsvampDen store del af forskningen relateret til syntese af målforbindelser blev udført af Polina Smirnova - en ph.d. studerende ved Institut for organisk kemi i SNS FEFU. Kredit:FEFUs pressekontor Kemi -
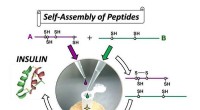 Højeffektiv syntese af insulin ved selvsamling baseret organisk kemiEn simpel protokol udviklet til insulinpræparation. Kredit:Michio Iwaoka Forskere ved Tokai, Osaka, Tohoku og Fukuoka Universiteter rapporterer i tidsskriftet Kommunikationskemi på syntese af in
Højeffektiv syntese af insulin ved selvsamling baseret organisk kemiEn simpel protokol udviklet til insulinpræparation. Kredit:Michio Iwaoka Forskere ved Tokai, Osaka, Tohoku og Fukuoka Universiteter rapporterer i tidsskriftet Kommunikationskemi på syntese af in -
 Beregning af overfladearealet af en terning:En klar, trin-for-trin guideAf Charlotte Johnson – Opdateret 24. marts 2022 En terning er en perfekt symmetrisk tredimensionel form:den har seks firkantede flader, otte hjørner og tolv kanter, der alle måler samme længde. Uanse
Beregning af overfladearealet af en terning:En klar, trin-for-trin guideAf Charlotte Johnson – Opdateret 24. marts 2022 En terning er en perfekt symmetrisk tredimensionel form:den har seks firkantede flader, otte hjørner og tolv kanter, der alle måler samme længde. Uanse
- Hvad har en dyrecelle?
- Hvorfor har du brug for at give universelt accepterede navne organismer?
- S. Koreas kimchi -underskud rammer rekordhøjt
- Forståelse af kold saltsyre (HCl):Egenskaber og sikkerhed
- Hvad er det første navn på Jorden?
- Hvem studerede kræfter og bevægelsen af objekter formulerede love bevægelse?


