Konverter mol til masse i kemi:En trin-for-trin guide
Af David Chandler
Opdateret 30. august 2022
I hverdagen bruger vi ofte ord som "dusin" eller "par" til at beskrive mængder. I kemi eksisterer et lignende koncept:muldvarpen (mol). Denne enhed repræsenterer 6.022×10 23 enheder, en værdi afledt af det nøjagtige antal atomer i 12g af isotopen kulstof-12. Ved at bruge molen kan en forbindelses molekylvægt tjene som en direkte omregningsfaktor mellem mol og gram.
Trin 1
Skriv den kemiske formel efterfulgt af antallet af mol. Formlen viser de atomer, der udgør et molekyle - for eksempel H₂O for vand. Placer mol-mængden før formlen og udelad enheden, når værdien er én. Således skrives 2molH2O som 2H2O, mens 1,8molH2O skrives som 1,8molH2O.
Trin 2
Beregn molekylvægten ved at tilføje atomvægtene af alle atomer i formlen. Atomvægte er angivet i det periodiske system. For vand, 2×1,008(⁴H)+16,00(⁸O)=18,02gmol⁻¹.
Trin 3
Multiplicer molekylvægten med antallet af mol for at opnå massen. For eksempel, 1 molH2O × 18,02 gmol-1 =18,02 g. 2 molH20 x 18,02 gmol-1 =36,04 g. En fraktioneret mængde, såsom 1,8 molH2O, giver 32,44 g.
Ting, der er nødvendige
- Periodisk tabel over elementerne
- Blyant
- Papir
 Varme artikler
Varme artikler
-
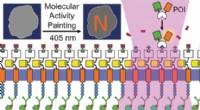 Molekylær aktivitet maleri til at kontrollere og overvåge switch-lignende, lyskontrollerede forsty…Kredit:Wiley Plasmamembranen tjener som et vigtigt knudepunkt for signalkaskader til styring af afgørende cellulære processer. Men det er et flydende medium, hvilket gør signaleringsprocesserne sv
Molekylær aktivitet maleri til at kontrollere og overvåge switch-lignende, lyskontrollerede forsty…Kredit:Wiley Plasmamembranen tjener som et vigtigt knudepunkt for signalkaskader til styring af afgørende cellulære processer. Men det er et flydende medium, hvilket gør signaleringsprocesserne sv -
 Harmløse elementer kan erstatte giftigt bly i elektronikHenrik Sønsteby holder en siliciumwafer dækket med en tynd film bestående af natrium, kalium, niobium og oxygen. Farverne er forårsaget af utilsigtede tykkelsesvariationer. Kredit:Bjarne Roesjoe/UiO
Harmløse elementer kan erstatte giftigt bly i elektronikHenrik Sønsteby holder en siliciumwafer dækket med en tynd film bestående af natrium, kalium, niobium og oxygen. Farverne er forårsaget af utilsigtede tykkelsesvariationer. Kredit:Bjarne Roesjoe/UiO -
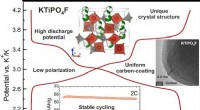 Forskere udvikler et nyt katodemateriale til metal-ion-batterierForskere fra Skoltech Center for Energy Science and Technology (CEST) skabte et nyt katodemateriale baseret på titaniumfluoridfosfat, hvilket muliggjorde opnåelse af overlegen energiydelse og stabil d
Forskere udvikler et nyt katodemateriale til metal-ion-batterierForskere fra Skoltech Center for Energy Science and Technology (CEST) skabte et nyt katodemateriale baseret på titaniumfluoridfosfat, hvilket muliggjorde opnåelse af overlegen energiydelse og stabil d -
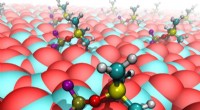 Videnskaben bag syltede batterielektrolytterHer er syltede elektrolytmolekyler (PF 2 OSiMe 3 ) binding til reaktionscentre på katodeoverfladen. For bold-og-stok-molekylerne, der er fastgjort til katodeoverfladen, olivengrøn angiver fosfor (
Videnskaben bag syltede batterielektrolytterHer er syltede elektrolytmolekyler (PF 2 OSiMe 3 ) binding til reaktionscentre på katodeoverfladen. For bold-og-stok-molekylerne, der er fastgjort til katodeoverfladen, olivengrøn angiver fosfor (
- Hvor er jernoxid på det periodiske tabel?
- Tvinge modsat mod bevægelse af en overflade over en anden?
- Tror du, at du har en hjernerystelse? En blodprøve kunne diagnosticere det
- Hvordan er genteori relateret til evolution?
- Hvordan en ER-simulering hjælper medicin- og ingeniørstuderende med at se nye synspunkter
- Hvad sker der, hvis du ikke spiser nok energi?


