Isotoper:At forstå atomer med det samme antal protoner
Her er hvorfor:
* Atomnummer: Dette repræsenterer antallet af protoner i et atoms kerne. Det definerer elementet. For eksempel har alle kulstofatomer 6 protoner.
* Massenummer: Dette repræsenterer det samlede antal protoner og neutroner i et atoms kerne. Neutroner bidrager også til massen af et atom.
Isotoper har samme antal protoner (atomnummer), men forskelligt antal neutroner. Det betyder, at de er det samme element, men har forskellige masser.
Eksempel:
* Carbon-12: 6 protoner og 6 neutroner (massenummer 12)
* Carbon-14: 6 protoner og 8 neutroner (massenummer 14)
Begge er kulstof (samme atomnummer), men kulstof-14 er tungere på grund af de ekstra neutroner.
Nøglepunkter:
* Isotoper af et grundstof har de samme kemiske egenskaber, fordi de har det samme antal elektroner og dermed den samme elektroniske konfiguration.
* Isotoper er almindelige og spiller vigtige roller på forskellige områder, herunder nuklear kemi, dating og medicin.
 Varme artikler
Varme artikler
-
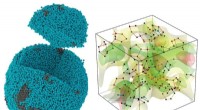 3D-billedundersøgelse afslører, hvordan atomer er pakket i amorfe materialerEksperimentelt 3D-atombillede af en lille, ikke-krystallinsk palladiumpartikel (venstre), hvor den 10-sidede femkantede bipyramide (til højre) er det mest udbredte motiv for, hvordan atomer pakker sam
3D-billedundersøgelse afslører, hvordan atomer er pakket i amorfe materialerEksperimentelt 3D-atombillede af en lille, ikke-krystallinsk palladiumpartikel (venstre), hvor den 10-sidede femkantede bipyramide (til højre) er det mest udbredte motiv for, hvordan atomer pakker sam -
 Når flere knogledannende celler er lig med mindre knogleForskere ved UConn Health har vist, hvordan et muteret gen forårsager overskydende knogleresorption i en sjælden knoglesygdom kendt som Lehmans syndrom. Deres forskning er forsideartiklen i 7. septemb
Når flere knogledannende celler er lig med mindre knogleForskere ved UConn Health har vist, hvordan et muteret gen forårsager overskydende knogleresorption i en sjælden knoglesygdom kendt som Lehmans syndrom. Deres forskning er forsideartiklen i 7. septemb -
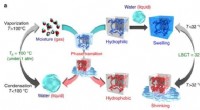 Forskere rapporterer om en temperaturfølsom gel, der absorberer og frigiver fugtIllustration af hovedbegreberne beskrevet i dette papir. Kredit:Kansai University Takashi Miyata ved Kansai University og kolleger melder ind Naturkommunikation en temperaturfølsom gel, der abso
Forskere rapporterer om en temperaturfølsom gel, der absorberer og frigiver fugtIllustration af hovedbegreberne beskrevet i dette papir. Kredit:Kansai University Takashi Miyata ved Kansai University og kolleger melder ind Naturkommunikation en temperaturfølsom gel, der abso -
 Nydesignede ligander til en katalytisk reaktion til syntetisering af lægemidler og nyttige forbinde…Tetrasubstituerede kromanoner er nyttige til lægemiddeldesign, men en effektiv strategi for deres generation har manglet indtil nu. Kredit:Gwangju Institute of Science and Technology I øjeblikket,
Nydesignede ligander til en katalytisk reaktion til syntetisering af lægemidler og nyttige forbinde…Tetrasubstituerede kromanoner er nyttige til lægemiddeldesign, men en effektiv strategi for deres generation har manglet indtil nu. Kredit:Gwangju Institute of Science and Technology I øjeblikket,


