Fluors unikke reaktivitet:hvorfor det reagerer med xenon, ikke jod
1. Elektronegativitet og ioniseringsenergi:
* Fluor: Fluor er det mest elektronegative element, hvilket betyder, at det har en stærk tendens til at tiltrække elektroner. Det har også en meget høj ioniseringsenergi, hvilket betyder, at det er svært at fjerne en elektron fra et fluoratom.
* Xenon: Xenon er en ædelgas og har en relativt lav ioniseringsenergi, hvilket gør det nemmere at fjerne en elektron fra et xenonatom.
2. Fluoreffekten:
* Fluor er utroligt reaktivt på grund af dets høje elektronegativitet og lille størrelse. Det kan overvinde ædelgaskonfigurationen af xenon og danne en binding. Dette er kendt som "fluoreffekten."
3. Jod vs. fluor:
* Jod: Mens jod også er et halogen, er det meget mindre elektronegativt end fluor. Den har også en større atomradius, hvilket betyder, at dens ydre elektroner er længere fra kernen og mindre fast holdt.
* Manglende reaktivitet: Jod mangler den nødvendige elektronegativitet og har ikke "fluoreffekten" til at overvinde den stabile elektroniske konfiguration af xenon.
Opsummering: Den vigtigste forskel ligger i den relative elektronegativitet og ioniseringsenergier af de involverede elementer. Fluors ekstraordinære reaktivitet og evne til at overvinde ædelgaskonfigurationen gør det muligt for det at reagere med xenon, mens jod mangler disse egenskaber.
Sidste artikelForståelse af atomblandinger:definition og eksempler
Næste artikelIsotoper:At forstå atomer med det samme antal protoner
 Varme artikler
Varme artikler
-
 Forskere skaber en ny type intelligent materialeTeamet, der skabte 2D-elektrolytterne, blev ledet af prof. Antonio Castro Neto (til højre), Direktør for CA2DM. Med ham er fru Mariana Costa (til venstre), publikationens første forfatter. Kredit:Nati
Forskere skaber en ny type intelligent materialeTeamet, der skabte 2D-elektrolytterne, blev ledet af prof. Antonio Castro Neto (til højre), Direktør for CA2DM. Med ham er fru Mariana Costa (til venstre), publikationens første forfatter. Kredit:Nati -
 Hvordan stabilisering af forstyrrede proteiner kan føre til den næste generation af medicinske app…LCST IDPPer udviser en bred vifte af hysteretisk faseadfærd. (A) Analyse af den reversible faseadfærd af LCST IDPPer i vores bibliotek afslørede tre grupper af gentagne motiver, hvor motiver i hver gr
Hvordan stabilisering af forstyrrede proteiner kan føre til den næste generation af medicinske app…LCST IDPPer udviser en bred vifte af hysteretisk faseadfærd. (A) Analyse af den reversible faseadfærd af LCST IDPPer i vores bibliotek afslørede tre grupper af gentagne motiver, hvor motiver i hver gr -
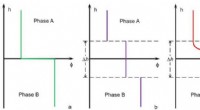 Forskere afslører naturen af jordvand og dets faseovergangFig. 1. De abstrakte grænseflademodeller mellem fase A og fase B. a:den skarpe Gibbs-grænseflademodel; b:den ensartede grænseflademodel; c:modellen med diffuse grænseflader. h er grænsefladetykkelsen.
Forskere afslører naturen af jordvand og dets faseovergangFig. 1. De abstrakte grænseflademodeller mellem fase A og fase B. a:den skarpe Gibbs-grænseflademodel; b:den ensartede grænseflademodel; c:modellen med diffuse grænseflader. h er grænsefladetykkelsen. -
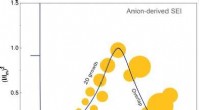 Anioner og opløsningsmidler styrer kernedannelse og vækst af den faste elektrolyt-interfase© Wiley-VCH. Kredit:Angewandte Chemie International Edition doi.org/10.1002/anie.202100494 Batterier oplades og genoplades - tilsyneladende alt sammen takket være et perfekt samspil mellem elektro
Anioner og opløsningsmidler styrer kernedannelse og vækst af den faste elektrolyt-interfase© Wiley-VCH. Kredit:Angewandte Chemie International Edition doi.org/10.1002/anie.202100494 Batterier oplades og genoplades - tilsyneladende alt sammen takket være et perfekt samspil mellem elektro
- Er vores sol en lille medium eller stor stjerne?
- Kortlægning af koraller fra himlen styrer revets bevarelse
- Forskere undersøger stjernepopulationer i den centrale region i Andromeda -galaksen
- 'Forstå videnskab'-webstedet præciserer, hvad videnskab er, ikke er
- Hvilket er det første trin, der fandt sted i artsdannelse af Galapagos-finker a. etablering af gene…
- Hvor mange kendte satellitter er gået til Mars?


