Kobber(II)sulfatpentahydrat:Farveændring ved opvarmning - Forklaring og videnskab
* Hydreret vs. vandfri: Den blå farve af kobber(II)sulfatpentahydrat opstår fra samspillet mellem vandmolekyler og kobberionerne. Denne interaktion skaber en specifik krystalstruktur, der absorberer visse bølgelængder af lys, hvilket resulterer i den blå farve.
* Dehydrering: Når du opvarmer kobber(II)sulfatpentahydrat, fjerner du i det væsentlige vandmolekylerne (dehydrering). Varmen giver nok energi til at bryde bindingerne, der holder vandmolekylerne til kobberionerne.
* Farveændring: Efterhånden som vandmolekylerne går tabt, ændres krystalstrukturen, og samspillet mellem kobberioner og vandmolekyler forstyrres. Dette fører til en ændring i den måde, lys absorberes på, hvilket resulterer i tab af den blå farve. Det resulterende vandfri kobber(II)sulfat (CuSO4) er hvidt.
Opsummering: Den blå farve af kobber(II)sulfatpentahydrat er et resultat af tilstedeværelsen af vandmolekyler. Når disse vandmolekyler fjernes ved opvarmning, mister forbindelsen sin blå farve og bliver hvid.
Sidste artikelMembranproteiner:Nøglen til kemiske reaktioner - forklaret
Næste artikelKobbersulfat i vand:Forstå løsninger og opløsning
 Varme artikler
Varme artikler
-
 Forskere opdager nye og skadelige kobber-proteinkomplekserKredit:TU Delft Kobber er vigtigt for mange processer i vores krop. Det understøtter produktionen af røde blodlegemer, stofskifte, og dannelsen af bindevæv og knogler, blandt andet. Kobber er
Forskere opdager nye og skadelige kobber-proteinkomplekserKredit:TU Delft Kobber er vigtigt for mange processer i vores krop. Det understøtter produktionen af røde blodlegemer, stofskifte, og dannelsen af bindevæv og knogler, blandt andet. Kobber er -
 Brug af en porøs porphyrin til at genvinde ædle metaller fra elektronisk affaldPorøs porfyrinpolymer (COP-180) kan udvinde guld fra et computerkredsløb og producere rene guldklumper. Kredit:Yeongran Hong Et internationalt hold af forskere har brugt en porøs porphyrin til at
Brug af en porøs porphyrin til at genvinde ædle metaller fra elektronisk affaldPorøs porfyrinpolymer (COP-180) kan udvinde guld fra et computerkredsløb og producere rene guldklumper. Kredit:Yeongran Hong Et internationalt hold af forskere har brugt en porøs porphyrin til at -
 Ny type elektrolyt kan forbedre superkondensatorens ydeevneStore anioner med lange haler (blå) i ioniske væsker kan få dem til at samle sig selv til sandwichlignende dobbeltlagsstrukturer på elektrodeoverflader. Ioniske væsker med sådanne strukturer har meget
Ny type elektrolyt kan forbedre superkondensatorens ydeevneStore anioner med lange haler (blå) i ioniske væsker kan få dem til at samle sig selv til sandwichlignende dobbeltlagsstrukturer på elektrodeoverflader. Ioniske væsker med sådanne strukturer har meget -
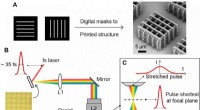 Ny teknik øger 3D-printhastigheden med 1, 000 til 10, 000 gangeFP-TPL baseret på rumlig og tidsmæssig fokusering. Kredit:CUHK Ultrapræcis 3-D printteknologi er en nøglemulighed for fremstilling af præcisionsbiomedicinske og fotoniske enheder. Imidlertid, den
Ny teknik øger 3D-printhastigheden med 1, 000 til 10, 000 gangeFP-TPL baseret på rumlig og tidsmæssig fokusering. Kredit:CUHK Ultrapræcis 3-D printteknologi er en nøglemulighed for fremstilling af præcisionsbiomedicinske og fotoniske enheder. Imidlertid, den
- Forskere forvandler køkkenaffald til biobrændstoffer
- Ny grøn teknologi genererer elektricitet ud af den blå luft
- Sådan bygger du et citronbatteri:Trin-for-trin-vejledning
- Hvad er begrænsninger i videnskaben?
- Billigere underlag lavet af oxidmaterialer
- Hvorfor udfører natriumchlorid elektricitet, når den er i flydende form, men ikke fast form?


