Svovlsyre:syre eller base? Forstå dens egenskaber
Her er hvorfor:
* Syrer donere protoner (H⁺-ioner) i opløsning.
* Baser acceptere protoner (H+-ioner) i opløsning.
Svovlsyre frigiver, når den er opløst i vand, H⁺-ioner, hvilket gør opløsningen mere sur:
H₂SO3 (vandigt) ⇌ H⁺ (vandigt) + HSO₃⁻ (vandigt)
Derfor er svovlsyre en svag syre, ikke en base.
 Varme artikler
Varme artikler
-
 Fra at lave vin til at håndtere mineaffald, ler er vigtigt for mange industrierDe unikke egenskaber ved ler gør dem velegnede til en lang række anvendelser. Kredit:Shutterstock Opdagelsen og brugen af ler går tilbage til 30, 000 år siden, gør ler til et af de ældste materi
Fra at lave vin til at håndtere mineaffald, ler er vigtigt for mange industrierDe unikke egenskaber ved ler gør dem velegnede til en lang række anvendelser. Kredit:Shutterstock Opdagelsen og brugen af ler går tilbage til 30, 000 år siden, gør ler til et af de ældste materi -
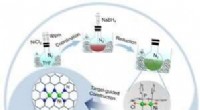 Forskere designer dinuclear-site katalysatorer og afslører den underliggende mekanismeSynteseskema. Kredit:DING Tao et al. Dinuclear-site katalysatorer (DSCer) har tiltrukket sig mere og mere opmærksomhed fra forskere på grund af deres fremragende katalytiske evne ved at inkorporer
Forskere designer dinuclear-site katalysatorer og afslører den underliggende mekanismeSynteseskema. Kredit:DING Tao et al. Dinuclear-site katalysatorer (DSCer) har tiltrukket sig mere og mere opmærksomhed fra forskere på grund af deres fremragende katalytiske evne ved at inkorporer -
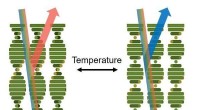 Farveændrende belægninger udløst af temperaturændringerFotoniske materialer har variable refleksionsegenskaber afhængigt af temperaturen. Kredit:Eindhoven University of Technology Farveskiftet kan påvirke vores opfattelse af objekter, bruges til at ad
Farveændrende belægninger udløst af temperaturændringerFotoniske materialer har variable refleksionsegenskaber afhængigt af temperaturen. Kredit:Eindhoven University of Technology Farveskiftet kan påvirke vores opfattelse af objekter, bruges til at ad -
 Flåtprotein hjælper antibiotika med at bekæmpe MRSA super bugKredit:stock.adobe.com Et protein afledt af flåter øger effektiviteten af antibiotikabehandling af methicillin-resistente Staphylococcus aureus, eller MRSA, ifølge en undersøgelse ledet af Yale.
Flåtprotein hjælper antibiotika med at bekæmpe MRSA super bugKredit:stock.adobe.com Et protein afledt af flåter øger effektiviteten af antibiotikabehandling af methicillin-resistente Staphylococcus aureus, eller MRSA, ifølge en undersøgelse ledet af Yale.
- Forskere skaber en schweizisk hærkniv til elektronstråler
- Hvor langt er Jorden fra Venus? Afstande, ligheder og missioner
- Mens Europa taler hårdt om klimaet, data viser, at emissionerne steg
- Hvordan solbær kunne hjælpe med at afslutte dårlige (for planeten) hårdage
- Hvornår bruges fysik i afsaltning?
- Hvorfor bøjer lysstrålen sig?


