Forståelse af kemiske ligningskoefficienter:Balanceringsreaktioner forklaret
* Bevarelse af messen: Det grundlæggende princip bag afbalancering af kemiske ligninger er loven om bevarelse af masse. Denne lov siger, at stof ikke kan skabes eller ødelægges i en kemisk reaktion. Den samlede masse af reaktanterne (de stoffer, der starter reaktionen) skal svare til den samlede masse af produkterne (de stoffer, der dannes ved reaktionen).
* Repræsenterer atomer: Kemiske formler repræsenterer typer og antal af atomer i et molekyle. For eksempel repræsenterer H2O et molekyle vand indeholdende to hydrogenatomer og et oxygenatom.
* Ændring af antallet af molekyler: Ændring af koefficienten foran en kemisk formel ændrer ikke selve den kemiske formel. I stedet ændrer det antallet af molekyler af det stof, der er involveret i reaktionen. For eksempel betyder 2H2O to molekyler vand.
Sådan fungerer det:
1. Start med en ubalanceret ligning: Denne ligning viser reaktanterne og produkterne, men har ikke det korrekte antal atomer på hver side.
2. Juster koefficienter: Ved at ændre koefficienterne foran de kemiske formler justerer du antallet af atomer i hvert grundstof på begge sider af ligningen.
3. Balancer atomerne: Du sigter efter at have det samme antal atomer af hvert grundstof på reaktantsiden og produktsiden.
Eksempel:
Ubalanceret ligning: H2 + O2 -> H20
Balanceret ligning: 2H2 + O2 -> 2H20
I den balancerede ligning justerede vi koefficienterne:
* 2 foran H₂ (reaktant)
* 2 foran H₂O (produkt)
Dette sikrer, at der er 4 brintatomer og 2 oxygenatomer på begge sider af ligningen, hvilket opretholder loven om bevarelse af masse.
Opsummering: Koefficienter i kemiske ligninger er essentielle for at afbalancere ligningen, som sikrer, at antallet af atomer i hvert grundstof er ens på begge sider, hvilket afspejler princippet om bevarelse af masse i kemiske reaktioner.
Sidste artikelSvovlsyre:syre eller base? Forstå dens egenskaber
Næste artikelK2CO3 kemisk formel:Forståelse af kaliumcarbonat
 Varme artikler
Varme artikler
-
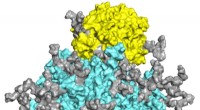 Ofte overset, molekyler kaldet glykaner regulerer COVID-19-spidsproteinfunktionenEn molekylær model viser det stærkt glykosylerede SARS-CoV-2-spidsprotein (cyan, med glykaner i grå og andre farver) bundet til den cellulære ACE2-receptor (gul). En ny undersøgelse fremhæver den krit
Ofte overset, molekyler kaldet glykaner regulerer COVID-19-spidsproteinfunktionenEn molekylær model viser det stærkt glykosylerede SARS-CoV-2-spidsprotein (cyan, med glykaner i grå og andre farver) bundet til den cellulære ACE2-receptor (gul). En ny undersøgelse fremhæver den krit -
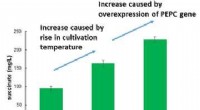 Verdens mest effektive produktion af succinat fra kuldioxidFigur 1:Øgede mængder succinat produceres baseret på overekspression af PEPC -gener og forhøjelse af dyrkningstemperaturen. Kredit:Kobe University Succinat bruges i vid udstrækning som en rå ingre
Verdens mest effektive produktion af succinat fra kuldioxidFigur 1:Øgede mængder succinat produceres baseret på overekspression af PEPC -gener og forhøjelse af dyrkningstemperaturen. Kredit:Kobe University Succinat bruges i vid udstrækning som en rå ingre -
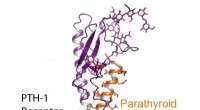 Fra receptorstruktur til nye osteoporoselægemidlerReceptoren er den vigtigste regulatoriske kontakt, der kontrollerer calciumfrigivelse fra knogler, og dermed et primært mål for udvikling af nye lægemidler til behandling af osteoporose. Receptoren be
Fra receptorstruktur til nye osteoporoselægemidlerReceptoren er den vigtigste regulatoriske kontakt, der kontrollerer calciumfrigivelse fra knogler, og dermed et primært mål for udvikling af nye lægemidler til behandling af osteoporose. Receptoren be -
 Dyb læring muliggør tidlig påvisning og klassificering af levende bakterier ved hjælp af hologra…Dyb læringsbaseret tidlig påvisning og klassificering af levende bakterier. en, Skematisk af enheden. b, Helpladebillede af E. coli og K. aerogenes kolonier. c, Eksempelbilleder af de individuelle vok
Dyb læring muliggør tidlig påvisning og klassificering af levende bakterier ved hjælp af hologra…Dyb læringsbaseret tidlig påvisning og klassificering af levende bakterier. en, Skematisk af enheden. b, Helpladebillede af E. coli og K. aerogenes kolonier. c, Eksempelbilleder af de individuelle vok
- Hvad er energien fra en foton, hvis bølgelængde 400nm?
- Solar Orbiter skal afsløre Suns hemmeligheder
- Storslået spiralgalakse strækkes af forbipasserende nabo
- En dag til at fejre kemiens yndlingsenhed - muldvarpen. Men hvad er en muldvarp?
- Hvilken type energi er Ice Cube?
- Centripetal Force: Hvad er det & hvorfor det betyder noget (m /ligning & eksempler)


