Spontane reaktioner:Forståelse af endoterme vs. eksoterme processer
* Spontane reaktioner: Disse reaktioner sker af sig selv uden behov for kontinuerlig ekstern energitilførsel. De har en tendens til at fortsætte mod en lavere energitilstand.
* Endotermiske reaktioner: Disse reaktioner absorberer varme fra deres omgivelser. Det betyder, at de kræver en tilførsel af energi for at opstå.
Hvorfor endoterme reaktioner ikke er spontane:
* Termodynamik: Spontaniteten af en reaktion er styret af et koncept kaldet Gibbs Free Energy (ΔG). For at en reaktion skal være spontan, skal ΔG være negativ.
* ΔG-ligning: ΔG =ΔH - TΔS
* ΔH er entalpiændringen (varme absorberet eller frigivet)
* T er temperaturen i Kelvin
* ΔS er entropiændringen (ændring i uorden)
* Endotermiske reaktioner og ΔG: Da endoterme reaktioner har en positiv ΔH (de absorberer varme), kan ΔG-værdien kun være negativ, hvis entropiændringen (ΔS) er stor nok, og temperaturen er høj nok til at overvinde den positive ΔH.
Eksempler på endoterme reaktioner:
* Smeltende is: Kræver varme for at bryde bindingerne, der holder vandmolekylerne i fast tilstand.
* Fotosyntese: Planter absorberer sollys for at omdanne kuldioxid og vand til glukose og ilt.
Vigtig bemærkning: Mens endoterme reaktioner generelt ikke er spontane under standardbetingelser, kan de fås til at forekomme med tilførsel af tilstrækkelig energi. Denne energi kan leveres af:
* Varme: At hæve temperaturen kan give den aktiveringsenergi, der er nødvendig for at overvinde energibarrieren.
* Andre energiformer: Lys, elektricitet eller mekanisk energi kan også drive endoterme reaktioner.
Sidste artikelSølvklorid (AgCl):Forståelse af ionsammensætning og iontal
Næste artikelSvovlsyre:syre eller base? Forstå dens egenskaber
 Varme artikler
Varme artikler
-
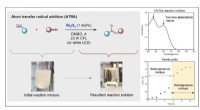 Lysere fremtiden for halvlederbaserede fotokatalytiske processerAtom transfer radikal addition (ATRA) reaktion mellem diethylbrommalonat (DEBM) og 5-hexen-1-ol som en reaktionsmodel. Kredit:Dr. Paola Riente Et samarbejde mellem Pericàs-gruppen med Prof. Timoth
Lysere fremtiden for halvlederbaserede fotokatalytiske processerAtom transfer radikal addition (ATRA) reaktion mellem diethylbrommalonat (DEBM) og 5-hexen-1-ol som en reaktionsmodel. Kredit:Dr. Paola Riente Et samarbejde mellem Pericàs-gruppen med Prof. Timoth -
 Ny bakterie- og algeproces kan hjælpe med at dekarbonisere britisk militærEn ny biologisk ingeniørproces, der kan hjælpe med at dekarbonisere det britiske militær, skal udvikles af forskere ved University of Sheffield. Den banebrydende forskning, ledet af akademikere fra U
Ny bakterie- og algeproces kan hjælpe med at dekarbonisere britisk militærEn ny biologisk ingeniørproces, der kan hjælpe med at dekarbonisere det britiske militær, skal udvikles af forskere ved University of Sheffield. Den banebrydende forskning, ledet af akademikere fra U -
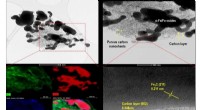 Adsorberende materiale udviklet fra PET -flasker til fjernelse af antibiotika fra vandKIST -forskerholdet observerede magnetiske porøse kulstofkompositmaterialer i transmissionselektronmikroskopet. Forskere testede effektiviteten af det porøse kulstofkomposit med hensyn til dets evne
Adsorberende materiale udviklet fra PET -flasker til fjernelse af antibiotika fra vandKIST -forskerholdet observerede magnetiske porøse kulstofkompositmaterialer i transmissionselektronmikroskopet. Forskere testede effektiviteten af det porøse kulstofkomposit med hensyn til dets evne -
 Borat bioaktivt glas i nanoskala:Et næste generations materiale til hudhelingBorat bioaktivt glas i nanoskala. Kredit:MA Kun For nylig, ved hjælp af en steady-state stærk magnetfelt eksperimentel enhed, forskere konstruerede bioaktivt boratglas i nanoskala (Nano-HCA@BG), s
Borat bioaktivt glas i nanoskala:Et næste generations materiale til hudhelingBorat bioaktivt glas i nanoskala. Kredit:MA Kun For nylig, ved hjælp af en steady-state stærk magnetfelt eksperimentel enhed, forskere konstruerede bioaktivt boratglas i nanoskala (Nano-HCA@BG), s
- Skaber kaos:Kratere og kollaps på Mars
- Hvem udførte først nøjagtige målinger af Orbit Mars?
- Bølgerne af energi, som et jordskælv producerer?
- Hvad er den blinkende stjerne på himlen i aften?
- Bliv menneske igen for at adressere sociale, miljømæssige udfordringer
- Forklar, hvorfor en centripetalkraft ikke fungerer på cirkulært bevægende objekt?


