Metallisk binding forklaret:Elektronhav og egenskaber
Metallisk binding er en type kemisk binding, der opstår mellem atomer af metalliske grundstoffer, karakteriseret ved et "hav" af delokaliserede elektroner, der er delt mellem alle atomerne i det metalliske gitter.
Her er en oversigt over, hvorfor dette er den bedste beskrivelse:
* Delokaliserede elektroner: Ved metallisk binding er valenselektronerne ikke tæt bundet til individuelle atomer. I stedet er de frie til at bevæge sig gennem hele metalgitteret. Dette skaber et "hav" af elektroner, der deles af alle metalatomerne.
* Metalgitter: Metaller findes i en krystalstruktur kendt som et metallisk gitter, hvor atomer er tæt pakket sammen. Denne struktur gør det muligt for elektronerne at bevæge sig frit og nemt.
* Stærke bånd: De delokaliserede elektroner skaber stærke tiltrækningskræfter mellem de positivt ladede metalioner, hvilket resulterer i stærke metalliske bindinger.
Andre nøglekarakteristika ved metallisk binding:
* Høj elektrisk ledningsevne: Den frie bevægelse af elektroner gør det muligt for metaller at lede elektricitet meget godt.
* Høj varmeledningsevne: Den frie bevægelse af elektroner gør det muligt for metaller at overføre varme effektivt.
* Smidbarhed og duktilitet: "Havet" af elektroner tillader metalatomer at glide forbi hinanden uden at bryde bindingerne, hvilket gør metaller formbare (kan hamres til plader) og duktile (kan trækkes ind i ledninger).
* Lyster: Metaller har ofte et skinnende udseende på grund af den måde, de interagerer med lys på.
 Varme artikler
Varme artikler
-
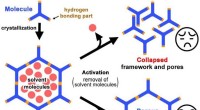 Porøse materialer kaster lys over miljørensningFigur 1. Skematisk fremstilling af porøse rammer konstrueret af brintmolekyler. Rammerne skal være stabile, selv efter fjernelse af opløsningsmiddelmolekyler fra porerne. Kredit:Osaka University I
Porøse materialer kaster lys over miljørensningFigur 1. Skematisk fremstilling af porøse rammer konstrueret af brintmolekyler. Rammerne skal være stabile, selv efter fjernelse af opløsningsmiddelmolekyler fra porerne. Kredit:Osaka University I -
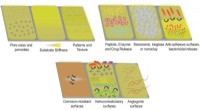 Polymerbaserede belægninger på metalliske implantater forbedrer knogleimplantatintegrationNaturlige polymerbelægninger på en metallisk implantatoverflade kan tilvejebringe et flerfunktionsinterfaselag til understøttelse af knogleimplantatintegration gennem skræddersyede egenskaber. Kredit:
Polymerbaserede belægninger på metalliske implantater forbedrer knogleimplantatintegrationNaturlige polymerbelægninger på en metallisk implantatoverflade kan tilvejebringe et flerfunktionsinterfaselag til understøttelse af knogleimplantatintegration gennem skræddersyede egenskaber. Kredit: -
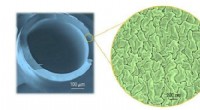 Oprydning med celluloseHoldet skabte velformede hulfibermembraner af cellulose til adskillelse af olie-i-vand-blandinger. Kredit:KAUST Selektivt permeable membraner fremstillet af fornybare plantebaserede materialer kan
Oprydning med celluloseHoldet skabte velformede hulfibermembraner af cellulose til adskillelse af olie-i-vand-blandinger. Kredit:KAUST Selektivt permeable membraner fremstillet af fornybare plantebaserede materialer kan -
 Hvordan de første biomolekyler kunne være blevet dannetKredit:Unsplash/CC0 Public Domain De kemiske forstadier til nutidens biomolekyler kunne være dannet ikke kun i dybhavet ved hydrotermiske åbninger, men også i varme damme på jordens overflade. De k
Hvordan de første biomolekyler kunne være blevet dannetKredit:Unsplash/CC0 Public Domain De kemiske forstadier til nutidens biomolekyler kunne være dannet ikke kun i dybhavet ved hydrotermiske åbninger, men også i varme damme på jordens overflade. De k
- At studere radioaktivt aluminium i stjernesystemer låser op for formationshemmeligheder
- Hvad hvis du malede et værelse med neglelak?
- Forskere afslører en ny rolle for mærkelige organismer i havets fødenet
- Hvad er formålet med ammoniumfosfat i gødning?
- Aktive hulrumssolitoner:Ultrastabile, optiske pulser med høj effekt til måling af lysbølger
- Holografisk billeddannelse af elektromagnetiske felter ved hjælp af elektronlys-kvanteinterferens


