Svovldioxid opløst i vand:syredannelse og kemisk reaktion
SO₂ (g) + H₂O (l) ⇌ H₂SO3 (vandig)
Denne reaktion er en ligevægtsreaktion, hvilket betyder, at den kan gå i begge retninger. Imidlertid er dannelsen af svovlsyrling begunstiget under normale forhold.
Svovlsyre er en svag syre, hvilket betyder, at den ikke ioniseres fuldt ud i vand. Det kan yderligere reagere med vand for at producere bisulfitioner (HSO₃⁻) og sulfitioner (SO₃²⁻):
H₂SO3 (aq) ⇌ H⁺ (aq) + HSO₃⁻ (aq)
HSO₃⁻ (aq) ⇌ H⁺ (aq) + SO₃²⁻ (aq)
Tilstedeværelsen af svovlsyrling i vandet bidrager til surheden af sur regn.
Sidste artikelBrintoxidationstal:Forståelse af +1 og -1
Næste artikelFysisk vs. kemisk forandring:Identifikation af forskelle og tegn
 Varme artikler
Varme artikler
-
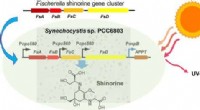 Gør dig klar til sommersolen med grønne solcremerKredit:American Chemical Society Selvom det har været en hård vinter for mange mennesker i USA, sommeren kommer. Og det betyder baggårdsgrill, sjov på stranden og selvfølgelig, sladder på solcreme
Gør dig klar til sommersolen med grønne solcremerKredit:American Chemical Society Selvom det har været en hård vinter for mange mennesker i USA, sommeren kommer. Og det betyder baggårdsgrill, sjov på stranden og selvfølgelig, sladder på solcreme -
 OLED'er bliver lysere og mere holdbareGrafik om at forbedre OLEDS på nanoskalaen. Kredit:Joan Rafols Ribé (UAB) og Paul Anton Will (TU Dresden) Organiske lysemitterende dioder (OLEDer) er modnet nok til at tillade de første kommerciel
OLED'er bliver lysere og mere holdbareGrafik om at forbedre OLEDS på nanoskalaen. Kredit:Joan Rafols Ribé (UAB) og Paul Anton Will (TU Dresden) Organiske lysemitterende dioder (OLEDer) er modnet nok til at tillade de første kommerciel -
 Hvad får en kæmpe vandmand til at stikke dødeligtKredit:CC0 Public Domain Med sommeren på vej, og nogle strande genåbner efter COVID-19-nedlukninger, folk vil tage til havet for at køle af på en varm dag. Men dem, der er uheldige nok til at stød
Hvad får en kæmpe vandmand til at stikke dødeligtKredit:CC0 Public Domain Med sommeren på vej, og nogle strande genåbner efter COVID-19-nedlukninger, folk vil tage til havet for at køle af på en varm dag. Men dem, der er uheldige nok til at stød -
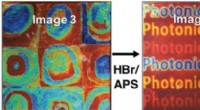 Teknik muliggør udskrivning og omskrivning af farvebillederDisse strukturelle farver blev trykt på det samme ark papir belagt med copolymerer ved anvendelse af ammoniumpersulfat og ethanol. Hydrogenbromid blev brugt til at neutralisere opløsningsmidlerne og o
Teknik muliggør udskrivning og omskrivning af farvebillederDisse strukturelle farver blev trykt på det samme ark papir belagt med copolymerer ved anvendelse af ammoniumpersulfat og ethanol. Hydrogenbromid blev brugt til at neutralisere opløsningsmidlerne og o
- Hvad er en anden mellem væv og kolonial organisme?
- Hvor lang tid med lysets hastighed ville det tage at få måne?
- Hvilke strukturer i plantecellen ses ikke Aniaml -celle?
- Selvsamlende nano-blæk danner ledende og gennemsigtige gitter under tryk
- Hvad hedder mønsterstjerner på himlen?
- Bærbar enhed til at snuse ud fangede mennesker


