Forståelse af kemiske bindinger:Hvordan elektronegativitet spiller en rolle
Elektronegativitet:
* Definition: Elektronegativitet er et mål for et atoms evne til at tiltrække elektroner mod sig selv, når det er i en kemisk binding.
* Tendenser: Elektronegativitet stiger generelt over en periode (fra venstre mod højre) og falder ned ad en gruppe (fra top til bund) på det periodiske system.
Obligationstyper og elektronegativitetsforskelle:
* Ikke-polære kovalente bindinger: Når elektronegativitetsforskellen mellem to atomer er meget lille (typisk mindre end 0,5), deles elektronerne ligeligt. Dette skaber en ikke-polær kovalent binding. Eksempel:Cl-Cl i klorgas (Cl2).
* Polære kovalente bindinger: Når elektronegativitetsforskellen mellem to atomer er moderat (mellem 0,5 og 1,7), deles elektronerne ulige. Dette skaber en polær kovalent binding, hvor det ene atom har en svagt negativ ladning (δ-) og det andet har en svagt positiv ladning (δ+). Eksempel:H-Cl i hydrogenchlorid (HCl).
* ioniske bindinger: Når elektronegativitetsforskellen mellem to atomer er stor (større end 1,7), overføres elektronerne i det væsentlige fra det ene atom til det andet. Dette skaber en ionbinding, hvilket resulterer i en positivt ladet kation og en negativt ladet anion. Eksempel:Na-Cl i natriumchlorid (NaCl).
Brug af elektronegativitet til at bestemme bindingstyper:
1. Find elektronegativitetsværdierne: Slå elektronegativitetsværdierne op for de to pågældende atomer. Du kan finde disse værdier i en lærebog, online eller i det periodiske system.
2. Beregn forskellen: Træk den mindre elektronegativitetsværdi fra den større.
3. Fortolk forskellen:
* Forskel <0,5:Ikke-polær kovalent binding
* 0,5
Vigtige overvejelser:
* Båndpolaritet: Jo større elektronegativitetsforskellen er, jo mere polær er bindingen. Det betyder, at der er en større adskillelse af ladning mellem atomerne.
* Forbindelsesstyrke: Ionbindinger er typisk stærkere end kovalente bindinger på grund af den fuldstændige overførsel af elektroner.
* Undtagelser: Der er nogle undtagelser fra disse regler, især for grundstoffer i midten af det periodiske system.
Eksempel:
Lad os betragte bindingen i kuldioxid (CO₂).
* Elektronegativitet af kulstof (C):2,55
* Elektronegativitet af ilt (O):3,44
Forskel =3,44 - 2,55 =0,89
Elektronegativitetsforskellen er mellem 0,5 og 1,7, så bindingerne i CO₂ er polær kovalent .
 Varme artikler
Varme artikler
-
 Forbindelse fra lægeurt dræber hjerneædende amøber i laboratorieundersøgelserBlade fra Inula viscosa , en flerårig middelhavsbusk, indeholder en forbindelse, der dræber hjerneædende amøber. Kredit:Tilpasset fra ACS Chemical Neuroscience 2020, DOI:10.1021/acschemneuro.0c006
Forbindelse fra lægeurt dræber hjerneædende amøber i laboratorieundersøgelserBlade fra Inula viscosa , en flerårig middelhavsbusk, indeholder en forbindelse, der dræber hjerneædende amøber. Kredit:Tilpasset fra ACS Chemical Neuroscience 2020, DOI:10.1021/acschemneuro.0c006 -
 En ny cermet, der kunne give en bedre varmeudveksling til solenergianlægEn nylig udvikling ville gøre elproduktion fra solens varme mere effektiv, ved at bruge keramiske metalplader til varmeoverførsel ved højere temperaturer og ved forhøjede tryk. Kredit:Purdue Universit
En ny cermet, der kunne give en bedre varmeudveksling til solenergianlægEn nylig udvikling ville gøre elproduktion fra solens varme mere effektiv, ved at bruge keramiske metalplader til varmeoverførsel ved højere temperaturer og ved forhøjede tryk. Kredit:Purdue Universit -
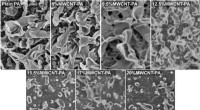 Forskere bruger kulstof nanorør-teknologi til at udvikle robuste vandafsaltningsmembranerSEM-billeder af MWCNT-PA (Multi-Walled Carbon Nanotube-Polyamide) nanokompositmembraner, for almindelig PA, og PA med 5, 9,5, 12,5, 15,5, 17 og 20 vægt% MWCNT, hvor de typiske laplignende strukturer o
Forskere bruger kulstof nanorør-teknologi til at udvikle robuste vandafsaltningsmembranerSEM-billeder af MWCNT-PA (Multi-Walled Carbon Nanotube-Polyamide) nanokompositmembraner, for almindelig PA, og PA med 5, 9,5, 12,5, 15,5, 17 og 20 vægt% MWCNT, hvor de typiske laplignende strukturer o -
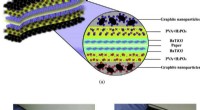 Formen på de kommende ting:Fleksibel, foldbare superkondensatorer til energilagring(a) skematisk af den symmetriske papirsuperkondensator med strukturen af GNPs elektroder (b) billede af den fremstillede superkondensator (c) billede af papirsuperkondensator i bøjetilstand. Kredit:
Formen på de kommende ting:Fleksibel, foldbare superkondensatorer til energilagring(a) skematisk af den symmetriske papirsuperkondensator med strukturen af GNPs elektroder (b) billede af den fremstillede superkondensator (c) billede af papirsuperkondensator i bøjetilstand. Kredit:
- Hvad er bruddet af større klipper i mindre stykker rock kaldet?
- Hvilken planet har en stor satellit sammenlignet med dens størrelse?
- Replikation af stuetemperatur-superlederkrav viser ikke superledning
- Hvad er slagkraften på en 100 kg objekt, der falder 2 meter?
- Subduktion af oceanisk litosfære under en kontinental blok giver anledning til hvilken type geologi…
- Hvordan relaterer ideerne om fordampning og kondens til tryktemperaturenergi?


