Forståelse af polære kovalente bindinger:Definition og forklaring
* Polære kovalente bindinger opstår, når to atomer med forskellige elektronegativitetsværdier deler elektroner. Elektronegativitet er et atoms evne til at tiltrække elektroner mod sig selv. Atomet med højere elektronegativitet vil trække de delte elektroner tættere på, hvilket skaber en delvis negativ ladning på det atom og en delvis positiv ladning på det andet atom.
Her er grunden til, at de andre muligheder er mindre nøjagtige:
* ioniske bindinger involverer fuldstændig overførsel af elektroner, hvilket skaber ioner med modsatte ladninger, der tiltrækkes af hinanden. Dette sker normalt mellem et metal og et ikke-metal.
* Ikke-polære kovalente bindinger opstår, når to atomer med lignende elektronegativitetsværdier deler elektroner ligeligt.
* Metalbindinger involvere et "hav af elektroner", hvor elektroner delokaliseres og deles mellem mange metalatomer.
Opsummering: En binding mellem to ulige atomer er sandsynligvis en polær kovalent binding på grund af den ulige deling af elektroner forårsaget af forskellen i elektronegativitet.
 Varme artikler
Varme artikler
-
 Billig chip-baseret enhed kan transformere spektrometriEn samling af mini-spektrometer-chips placeres på en bakke efter at være blevet fremstillet gennem konventionelle chip-fremstillingsprocesser. Kredit:Felice Frankel Spektrometre - enheder, der ske
Billig chip-baseret enhed kan transformere spektrometriEn samling af mini-spektrometer-chips placeres på en bakke efter at være blevet fremstillet gennem konventionelle chip-fremstillingsprocesser. Kredit:Felice Frankel Spektrometre - enheder, der ske -
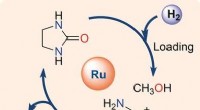 Kemisk brintlagringssystemKredit:Wiley Brint er en yderst attraktiv, men også stærkt eksplosiv energibærer, som kræver sikker, let og billig opbevaring samt transportsystemer. Forskere ved Weizmann Institute of Science, Is
Kemisk brintlagringssystemKredit:Wiley Brint er en yderst attraktiv, men også stærkt eksplosiv energibærer, som kræver sikker, let og billig opbevaring samt transportsystemer. Forskere ved Weizmann Institute of Science, Is -
 Ion billard cue ny materialesyntesemetodeEn skematisk illustration af den nyudviklede Proton-Driven Ion Introduction (PDII) metode. Protoner genereret ved elektrisk adskillelse af brint skydes ind i forsyningskilden for de ønskede ioner. Ion
Ion billard cue ny materialesyntesemetodeEn skematisk illustration af den nyudviklede Proton-Driven Ion Introduction (PDII) metode. Protoner genereret ved elektrisk adskillelse af brint skydes ind i forsyningskilden for de ønskede ioner. Ion -
 En kemisk omfavnelse fra den perfekte værtGengwu Zhang udfører adskillelseseksperimentet ved hjælp af to ekstraktionstårne. Kredit:© 2020 KAUST En industriel proces, der i øjeblikket bruger store mængder energi i petrokemiske anlæg rundt
En kemisk omfavnelse fra den perfekte værtGengwu Zhang udfører adskillelseseksperimentet ved hjælp af to ekstraktionstårne. Kredit:© 2020 KAUST En industriel proces, der i øjeblikket bruger store mængder energi i petrokemiske anlæg rundt
- Opfordringer til at forbyde "skadelig pornografi" er udbredte - her er, hvad teenagere rent faktisk …
- Til Arktis for CryoSat og videre
- Hvad er den kraft, der holder luft nær jordoverfladen kaldet?
- Hvordan leveres mad og energi til hudceller?
- Får den jordhalvkugle, der vippes væk fra solen, mindre direkte nedbør end andre modtager?
- Hvilke energikilder er mest sandsynligt rigeligt i Californien på grund af sin position på en plad…


