Forståelse af obligationstyper:Elektronegativitetens rolle
1. Forskellen i elektronegativitet:
* ioniske bindinger: Når elektronegativitetsforskellen mellem to atomer er stor (typisk større end 1,7), vil atomet med højere elektronegativitet effektivt "stjæle" elektronen(erne) fra det mindre elektronegative atom. Dette resulterer i dannelsen af ioner (positivt og negativt ladede atomer) og en elektrostatisk tiltrækning mellem dem, der danner en ionbinding.
* Kovalente bindinger: Når elektronegativitetsforskellen er lille (typisk mindre end 1,7), deler atomerne elektroner for at opnå en stabil elektronkonfiguration. Denne deling danner en kovalent binding.
2. Typer af kovalente bindinger:
* Ikke-polære kovalente bindinger: Når elektronegativitetsforskellen er meget lille (tæt på nul), elektronerne deles ligeligt mellem de to atomer. Dette resulterer i en ikke-polær kovalent binding.
* Polære kovalente bindinger: Når elektronegativitetsforskellen er moderat (mellem 0,5 og 1,7), deles elektronerne ulige. Atomet med højere elektronegativitet vil tiltrække de delte elektroner stærkere, hvilket resulterer i en let negativ ladning på det atom og en let positiv ladning på det andet. Dette skaber en polær kovalent binding med et dipolmoment.
Nøglepunkter at huske:
* Elektronegativitet er en relativ egenskab. Det fortæller dig ikke det absolutte "træk" på elektroner, men snarere hvor stærkt et atom tiltrækker elektroner sammenlignet med et andet atom.
* Jo større elektronegativitetsforskellen er, jo mere ionisk er bindingen.
* Jo mindre elektronegativitetsforskellen er, jo mere kovalent er bindingen.
* Elektronegativitetsværdier er angivet på en skala (f.eks. Pauling-skala). Du kan bruge disse værdier til at beregne elektronegativitetsforskellen mellem to atomer.
Eksempel:
* NaCl (natriumchlorid): Natrium (Na) har en elektronegativitet på 0,93, mens klor (Cl) har en elektronegativitet på 3,16. Forskellen er 2,23, hvilket indikerer en stor elektronegativitetsforskel. Derfor danner NaCl en ionbinding.
* H₂O (vand): Ilt (O) har en elektronegativitet på 3,44, mens hydrogen (H) har en elektronegativitet på 2,20. Forskellen er 1,24, hvilket indikerer en moderat elektronegativitetsforskel. Derfor danner H2O polære kovalente bindinger.
* H₂ (brint): Begge brintatomer har samme elektronegativitet (2,20). Elektronegativitetsforskellen er nul, hvilket fører til en ikke-polær kovalent binding.
Sammenfattende giver elektronegativitetsforskelle et værdifuldt værktøj til at forudsige den type binding, der vil dannes mellem to atomer, hvilket giver indsigt i molekylers natur og adfærd.
 Varme artikler
Varme artikler
-
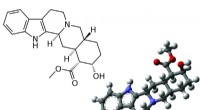 At finde ud af molekylernes 3D-form med et tryk på en knapEt computerprogram kan finde ud af 3D-strukturen (til højre) af molekyler som Yohimbine med et tryk på en knap. Molekyler med den samme 2-D struktur (venstre) kan have forskellige 3-D strukturer. Kred
At finde ud af molekylernes 3D-form med et tryk på en knapEt computerprogram kan finde ud af 3D-strukturen (til højre) af molekyler som Yohimbine med et tryk på en knap. Molekyler med den samme 2-D struktur (venstre) kan have forskellige 3-D strukturer. Kred -
 Knap ridser overfladen:En ny måde at lave robuste membraner påEn ny Argonne-teknik kan dyrke materiale inde i membranstrukturer, ændre deres kemi uden at påvirke poreformen markant. Dette giver forskere mulighed for at forbedre membraner på forskellige måder. Kr
Knap ridser overfladen:En ny måde at lave robuste membraner påEn ny Argonne-teknik kan dyrke materiale inde i membranstrukturer, ændre deres kemi uden at påvirke poreformen markant. Dette giver forskere mulighed for at forbedre membraner på forskellige måder. Kr -
 Påvisning af cyanideksponeringKredit:American Chemical Society Cyanideksponering kan ske erhvervsmæssigt eller i lave niveauer ved at indånde cigaretrøg - eller ved at blive forgiftet af nogen, der er ude for at få dig. Effekt
Påvisning af cyanideksponeringKredit:American Chemical Society Cyanideksponering kan ske erhvervsmæssigt eller i lave niveauer ved at indånde cigaretrøg - eller ved at blive forgiftet af nogen, der er ude for at få dig. Effekt -
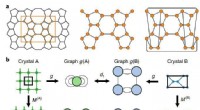 En ny matematisk tilgang til forståelse af zeolitterGraph og supercell matching. en, Repræsentation af en zeolit ved hjælp af en graf (til venstre). Enhedscellegrafen (midten) modificeres for at opfylde periodiske grænsebetingelser ved at sløjfe bind
En ny matematisk tilgang til forståelse af zeolitterGraph og supercell matching. en, Repræsentation af en zeolit ved hjælp af en graf (til venstre). Enhedscellegrafen (midten) modificeres for at opfylde periodiske grænsebetingelser ved at sløjfe bind


