Elektronegativitet og bindingspolaritet:Forståelse af kemiske bindinger
1. Elektronegativitetsforskel og bindingspolaritet:
* Elektronegativitet er et atoms evne i et molekyle til at tiltrække elektroner mod sig selv.
* Jo større forskellen er på elektronegativitet mellem to atomer, jo mere polær obligationen. Dette betyder, at elektronerne er ulige delt og bruger mere tid i nærheden af det mere elektronegative atom.
2. Typer af obligationer baseret på elektronegativitet:
* Ikke-polære kovalente bindinger: Når elektronegativitetsforskellen mellem to atomer er meget lille (typisk mindre end 0,5), deles elektronerne næsten ligeligt. Dette resulterer i en ikke-polær kovalent binding .
* Polære kovalente bindinger: Når elektronegativitetsforskellen er moderat (mellem 0,5 og 1,7), deles elektronerne ulige. Dette skaber en polær kovalent binding med delvise positive og delvise negative ladninger på atomerne.
* ioniske bindinger: Når elektronegativitetsforskellen er stor (typisk større end 1,7), det ene atom *tager* effektivt elektronen fra det andet. Dette skaber ioner med fulde positive og negative ladninger, hvilket fører til en ionisk binding .
3. Konsekvenser af bindingspolaritet:
* Molekylære dipolmomenter: Polære kovalente bindinger skaber et dipolmoment i et molekyle, hvilket betyder, at molekylet har en positiv og negativ ende. Dette påvirker molekylets interaktion med andre molekyler og dets generelle adfærd.
* Opløselighed: Polære molekyler har en tendens til at opløses i polære opløsningsmidler, mens ikke-polære molekyler opløses i ikke-polære opløsningsmidler.
* Kemisk reaktivitet: Bindingspolaritet påvirker molekylernes reaktivitet. For eksempel er polære molekyler mere tilbøjelige til at deltage i reaktioner, der involverer ladningsinteraktioner.
Opsummering:
Elektronegativitetsforskel dikterer direkte karakteren af en binding. Dette bestemmer deling af elektroner, skaber bindingspolaritet og påvirker molekylernes overordnede egenskaber og reaktivitet.
Sidste artikelCalciumsaltsyrereaktion:Kemisk ligning og forklaring
Næste artikelForståelse af obligationstyper:Elektronegativitetens rolle
 Varme artikler
Varme artikler
-
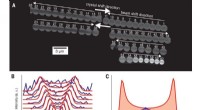 En måde at bestemme den absolutte stereokemi af små, organiske molekylerDiffraktionsdataindsamling og avanceret diffraktionsintensitetsekstraktion. (A) Scanning af krystal under dataindsamling. Stråle- og krystalforskydninger er angivet med hvide pile. (B) Plot af vippeku
En måde at bestemme den absolutte stereokemi af små, organiske molekylerDiffraktionsdataindsamling og avanceret diffraktionsintensitetsekstraktion. (A) Scanning af krystal under dataindsamling. Stråle- og krystalforskydninger er angivet med hvide pile. (B) Plot af vippeku -
 En mere sikker måde for politiet at teste narkotikabeviser påKredit:CC0 Public Domain Forskere har demonstreret en måde, hvorpå politiet hurtigt og sikkert kan teste, om en baggie eller anden pakke indeholder ulovlige stoffer uden at skulle håndtere noget m
En mere sikker måde for politiet at teste narkotikabeviser påKredit:CC0 Public Domain Forskere har demonstreret en måde, hvorpå politiet hurtigt og sikkert kan teste, om en baggie eller anden pakke indeholder ulovlige stoffer uden at skulle håndtere noget m -
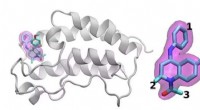 Forskningsgruppen bruger supercomputing til at målrette de mest lovende lægemiddelkandidater ud fr…En skematisk oversigt over BRD4 -proteinet bundet til et af 16 lægemidler baseret på det samme tetrahydroquinolin -stillads (fremhævet i magenta). Regioner, der er kemisk modificeret mellem de lægemid
Forskningsgruppen bruger supercomputing til at målrette de mest lovende lægemiddelkandidater ud fr…En skematisk oversigt over BRD4 -proteinet bundet til et af 16 lægemidler baseret på det samme tetrahydroquinolin -stillads (fremhævet i magenta). Regioner, der er kemisk modificeret mellem de lægemid -
 Beregningsstrategier overvinder hindringer i udviklingen af peptidterapiEn kunstners opfattelse af kraften ved beregningsmæssigt design til at udforske og belyse strukturerede peptider på tværs af det enorme energilandskab. Kredit:Vikram Mulligan/University of Washington
Beregningsstrategier overvinder hindringer i udviklingen af peptidterapiEn kunstners opfattelse af kraften ved beregningsmæssigt design til at udforske og belyse strukturerede peptider på tværs af det enorme energilandskab. Kredit:Vikram Mulligan/University of Washington
- Hvad er de individuelle enheder i DNA kendt som?
- Spørgsmål og svar med Jason Hong om svindel og andre sårbarheder under COVID-19-pandemien
- Vandkogende volumen fra 3 kJ:Forståelse af energikravet
- Hvilket af følgende er en brugsbakterie A.Preventing nedbrydning b. Nedbrydning af materialer c. ne…
- Chokoladefysik:Hvordan modellering kunne forbedre 'mundfornemmelsen'
- Forskere udvikler et nyt lægemiddel til kræftdiagnostik og behandling


