Beregningsstrategier overvinder hindringer i udviklingen af peptidterapi
En kunstners opfattelse af kraften ved beregningsmæssigt design til at udforske og belyse strukturerede peptider på tværs af det enorme energilandskab. Kredit:Vikram Mulligan/University of Washington Insittute for Protein Design
Nye beregningsstrategier rapporteret i denne uge i Videnskab kan hjælpe med at realisere løftet om peptidbaserede lægemidler. Peptider ligner proteinmolekyler, men adskiller sig i deres mindre størrelse, struktur og funktioner.
Makrocykliske peptider har vakt interesse i den farmaceutiske industri, fordi de har visse fysiske og kemiske egenskaber, der kan blive grundlaget for en ny generation af medicin.
Små peptider har fordelene ved lægemidler med små molekyler, som aspirin, og store antistofbehandlinger, ligesom rituximab, med færre ulemper. De er stabile som små molekyler og potente og selektive antistoffer.
Et eksempel på en succeshistorie med makrocyklisk peptidlægemiddel er cyclosporin, et immunsuppressivt middel til organtransplantationer og nogle autoimmune lidelser.
Før arbejdet beskrevet i Videnskab papir, der var ingen måde at systematisk designe ordnede peptidmakrocykler som cyclosporin.
Naturligt forekommende peptider, der kan tjene som pålidelige udgangspunkter, eller stilladser, er få. Lige så frustrerende er det, at de ofte ikke præsterer som forventet, når de bliver genbrugt. I stedet, forskere havde tyet til at screene store, tilfældigt genererede biblioteker af forbindelser i håbet om at finde det, de havde brug for.
De metoder, der er beskrevet i rapporten, "Omfattende beregningsdesign af ordnede peptidmakrocykler" løser nu disse problemer.
Denne konceptuelle illustration viser, hvordan peptidheteropolymerer kan programmeres fra mindre komponenter til at udforske et mangfoldigt energilandskab. Kredit:Ahmad Hosseinzadeh og Khosro Khosravi
Hovedforfatterne er Parisa Hossienzadeh, Gaurav Bhardwaj og Vikram Mulligan, fra University of Washington School of Medicine Department of Biochemistry og UW Institute of Protein Design. Seniorforfatteren er David Baker, professor i biokemi og leder af instituttet. Baker er også efterforsker ved Howard Hughes Medical Institute.
"I vores avis, " bemærkede forskerne, "Vi beskriver beregningsstrategier til at designe peptider, der antager forskellige former med meget høj nøjagtighed og for at give omfattende dækning af de strukturer, der kan dannes af korte peptider."
De påpegede fordelene ved denne nye beregningsmetode:
Først, de var i stand til at designe og kompilere et bibliotek af mange nye stabile peptidstilladser, der kan levere de grundlæggende platforme for lægemiddelkandidatarkitektur. Deres metoder kan også bruges til at designe yderligere brugerdefinerede peptider med vilkårlige former efter behov.
"Vi prøvede det mangfoldige landskab af former, som peptider kan danne, som en guide til at designe den næste generation af lægemidler, " sagde forskerne.
Nøglen til kontrol af molekylers geometri og kemi var designet af peptider med naturlige aminosyrer, kaldet L-aminosyrer, og deres spejlmodsætninger indeholdende D-aminosyrer. (L og D står for latinske ord for at rotere til venstre eller højre, da nogle molekylære strukturer kan have venstre- eller højrehåndethed eller chiralitet).
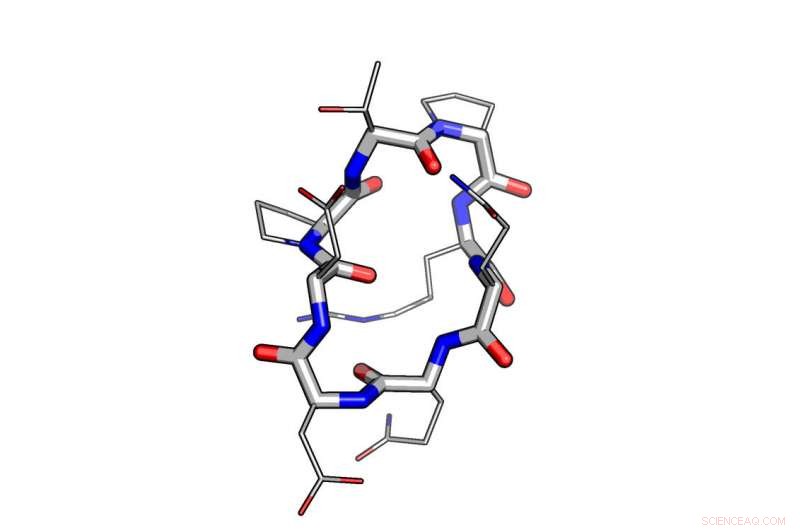
Et eksempel på brugen af computerdesign til modellering af et peptid. Kredit:University of Washington Institute for Protein Design
D-aminosyrerne forbedrede farmakologiske egenskaber ved at øge modstandsdygtigheden over for naturlige enzymer, der nedbryder peptider. Inkludering af D-aminosyrer i design giver også mulighed for et mere forskelligartet udvalg af former.
At designe peptider kræver intensiv computerkraft, resulterer i dyre beregninger. Forskerne krediterede en kadre af borgerforskere og frivillige, der donerede deres ekstra mobiltelefonminutter og computertid. Hyak Supercomputer ved University of Washington kørte også nogle af programmerne.
Forskerne pegede på fremtidige retninger for deres peptidberegningsdesigntilgange. De håber at designe peptider, der kan trænge igennem cellemembraner og gå ind i levende celler.
I andre aspekter, de planlægger at tilføje nye funktionaliteter til peptidstrukturer ved at stabilisere bindingsmotiverne ved protein-protein-grænseflader til grundlæggende videnskabelige undersøgelser. Til kliniske anvendelser, de forventer at bruge deres metoder og stilladser til at udvikle peptidbaserede lægemidler.
 Varme artikler
Varme artikler
-
 Læsning af histonmodifikationer, et onkoprotein modificeres til gengældPæren symboliserer TRIM24, et histone readerprotein, som binder kromatin. Chromatinassociation udløser signalering til TRIM24, markeret eller belyst af en post-translationel modifikation kaldet SUMOyl
Læsning af histonmodifikationer, et onkoprotein modificeres til gengældPæren symboliserer TRIM24, et histone readerprotein, som binder kromatin. Chromatinassociation udløser signalering til TRIM24, markeret eller belyst af en post-translationel modifikation kaldet SUMOyl -
 Team opdager molekylær kanal, der regulerer blodtrykketVed hjælp af et kryo-elektronmikroskop, forskere ved OHSU i Portland, Oregon, genereret en tredimensionel model af den humane epitheliale natriumkanal. Kanalen er kritisk til at kontrollere blodtrykke
Team opdager molekylær kanal, der regulerer blodtrykketVed hjælp af et kryo-elektronmikroskop, forskere ved OHSU i Portland, Oregon, genereret en tredimensionel model af den humane epitheliale natriumkanal. Kanalen er kritisk til at kontrollere blodtrykke -
 Biostasis har til formål at forhindre død efter traumatisk skade ved at bremse biokemiske reaktion…DARPAs Biostasis-program har til formål at forhindre død efter traumatisk skade ved at bremse biokemiske reaktioner inde i celler, dermed forlænge den gyldne time for medicinsk intervention. De ønsked
Biostasis har til formål at forhindre død efter traumatisk skade ved at bremse biokemiske reaktion…DARPAs Biostasis-program har til formål at forhindre død efter traumatisk skade ved at bremse biokemiske reaktioner inde i celler, dermed forlænge den gyldne time for medicinsk intervention. De ønsked -
 Skabelon til at skabe superatomer kunne give bedre batterierKredit:ktsdesign, Shutterstock Virginia Commonwealth University-forskere har opdaget en ny strategi til at skabe superatomer - kombinationer af atomer, der kan efterligne egenskaberne af mere end
Skabelon til at skabe superatomer kunne give bedre batterierKredit:ktsdesign, Shutterstock Virginia Commonwealth University-forskere har opdaget en ny strategi til at skabe superatomer - kombinationer af atomer, der kan efterligne egenskaberne af mere end
- Fødslen af massive stjerner er ledsaget af stærke lysstyrkeudbrud
- Palcacocha-isfald viser risikosårbarheder i Peru
- Har COVID 19 undermineret retsstaten? Ny forskning undersøger handlinger på det vestlige Balkan
- Team udvikler verdens første test på stedet for syntetiske krydderier
- Star Treks formel for bæredygtig byinnovation
- Forskelle mellem hydraulikmotorer og elmotorer


