Dobbelt-erstatningsreaktioner:Definition, eksempler og ligninger
Forstå dobbelterstatningsreaktioner
* Definition: I en dobbelt-erstatningsreaktion skifter de positive og negative ioner af to reaktanter plads.
* Generel formular: AB + CD → AD + CB
Eksempel
Lad os se på reaktionen mellem sølvnitrat (AgNO₃) og natriumchlorid (NaCl):
* Reaktanter:
* Sølvnitrat (AgNO₃):Ag⁺ (sølvion) + NO₃⁻ (nitration)
* Natriumchlorid (NaCl):Na⁺ (natriumion) + Cl⁻ (chloridion)
* Produkter:
* Sølvchlorid (AgCl):Ag⁺ (sølvion) + Cl⁻ (chloridion)
* Natriumnitrat (NaNO₃):Na⁺ (natriumion) + NO₃⁻ (nitration)
Balanceret ligning:
AgNO3(aq) + NaCl(aq) → AgCl(s) + NaNO3(aq)
Forklaring:
* Sølvionen (Ag⁺) fra sølvnitrat kombineres med chloridionen (Cl⁻) fra natriumchlorid og danner sølvchlorid (AgCl).
* Natriumionen (Na⁺) fra natriumchlorid kombineres med nitrationen (NO₃⁻) fra sølvnitrat for at danne natriumnitrat (NaNO₃).
Nøglefunktioner:
* To ioniske forbindelser reagerer.
* De positive og negative ioner skifter partner.
* Reaktionen sker normalt i vandig opløsning (opløst i vand).
* Ofte er ét produkt et bundfald (et fast stof, der dannes ud af opløsning). I vores eksempel er sølvchlorid (AgCl) et bundfald.
Sig til, hvis du vil se flere eksempler!
Sidste artikelOvergangsmetaller:Forstå flere ionladninger
Næste artikelEksempler på ionbinding:Forståelse af natriumchlorid og magnesiumoxid
 Varme artikler
Varme artikler
-
 En fortælling om hyrder og spiralerKrigsskade med konsekvenser:efter Anden Verdenskrig, Giuseppe Torrettis marmorrelief Tilbedelse af hyrderne overlevede kun i fragmenter (brunlige sektioner), som er vist her i kombination med et sort
En fortælling om hyrder og spiralerKrigsskade med konsekvenser:efter Anden Verdenskrig, Giuseppe Torrettis marmorrelief Tilbedelse af hyrderne overlevede kun i fragmenter (brunlige sektioner), som er vist her i kombination med et sort -
 Nyt materiale til katolytter og anolytter i organiske redoxflow-batterierKredit:CC0 Public Domain Forskere fra Skoltech og deres samarbejdspartnere har designet, syntetiserede og evaluerede nye forbindelser, der kan tjene som katolytter og anolytter til organiske redox
Nyt materiale til katolytter og anolytter i organiske redoxflow-batterierKredit:CC0 Public Domain Forskere fra Skoltech og deres samarbejdspartnere har designet, syntetiserede og evaluerede nye forbindelser, der kan tjene som katolytter og anolytter til organiske redox -
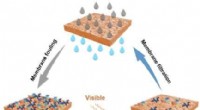 Forskere udvikler N-dopede selvrensende membraner, der bruger bestråling af synligt lysSkematisk diagram af N-TiO 2 og TiO 2 overtrukket membranforberedelse og mekanisme for synligt lysaktiveret fotokatalyse til begroningsbegrænsning. Kredit:ZHANG Huiru Forskere fra Institute of
Forskere udvikler N-dopede selvrensende membraner, der bruger bestråling af synligt lysSkematisk diagram af N-TiO 2 og TiO 2 overtrukket membranforberedelse og mekanisme for synligt lysaktiveret fotokatalyse til begroningsbegrænsning. Kredit:ZHANG Huiru Forskere fra Institute of -
 Forskere tager et fingerpeg fra naturen om at skabe skudsikre belægningerKredit:University of Houston Reje, hummer og svampe virker måske ikke som gode redskaber til slagmarken, men tre ingeniører fra University of Houston bruger kitin-et derivat af glukose, der findes
Forskere tager et fingerpeg fra naturen om at skabe skudsikre belægningerKredit:University of Houston Reje, hummer og svampe virker måske ikke som gode redskaber til slagmarken, men tre ingeniører fra University of Houston bruger kitin-et derivat af glukose, der findes
- Skal vi være nervøse over togrejser?
- Dårligt helbred øger chancen for recidiv og genfængsling
- Partnere i kriminalitet? Et historisk perspektiv på kumulativ ekstremisme Danmark
- Hvad er 3 gode ting ved fossile brændstoffer og dårlige ting?
- Hvilken værdi på pH-skalaen repræsenterer en stærk syrebase og neutralt stof?
- Forsker studerer, hvordan professionelle sportsfans bruger mobiltelefoner


