Overgangsmetaller:Forstå flere ionladninger
Her er hvorfor overgangsmetaller danner flere ioner:
* Variable oxidationstilstande: Overgangsmetaller har flere elektroner i deres d-orbitaler, som let kan tabes for at danne ioner. Antallet af tabte elektroner kan variere, hvilket fører til forskellige oxidationstilstande og dermed forskellige ladninger på ionen.
* Elektronkonfiguration: D-orbitalerne er relativt tæt på energi, hvilket giver mulighed for tab af elektroner fra forskellige energiniveauer. Denne fleksibilitet giver anledning til flere mulige ioniske ladninger.
Eksempler:
* Jern (Fe): Kan danne Fe²⁺ (jernholdige) og Fe³⁺ (jernholdige) ioner.
* Kobber (Cu): Kan danne Cu⁺ (kobber) og Cu²⁺ (kobber) ioner.
* Mangan (Mn): Kan danne Mn²⁺, Mn3⁺, Mn⁴⁺, Mn⁶⁺ og Mn⁷⁺ ioner.
Bemærk: Mens overgangsmetaller er den primære gruppe af grundstoffer, der danner flere ioner, kan nogle ikke-metaller også udvise variable oxidationstilstande og danne ioner med forskellige ladninger. For eksempel kan phosphor (P) danne P3⁻-, P⁵⁺- og P3⁺-ioner.
 Varme artikler
Varme artikler
-
 Forskere på forkant med udvikling af maskinlæringsmetoder til kemisk opdagelseKredit:CC0 Public Domain Opdagelsen og formuleringen af nye lægemidler, antivirale midler, antibiotika og generelt kemikalier med skræddersyede egenskaber er en lang og omhyggelig proces. Tværfa
Forskere på forkant med udvikling af maskinlæringsmetoder til kemisk opdagelseKredit:CC0 Public Domain Opdagelsen og formuleringen af nye lægemidler, antivirale midler, antibiotika og generelt kemikalier med skræddersyede egenskaber er en lang og omhyggelig proces. Tværfa -
 Mere effektive fotokatalysatorer kunne frigøre solenergiens potentiale(l-r) Jan Kosco, Iain McCulloch og Calvyn Howells diskuterer potentialet i deres brintudviklingsfotokatalysator. Kredit:KAUST En organisk halvlederfotokatalysator, der markant forbedrer generering
Mere effektive fotokatalysatorer kunne frigøre solenergiens potentiale(l-r) Jan Kosco, Iain McCulloch og Calvyn Howells diskuterer potentialet i deres brintudviklingsfotokatalysator. Kredit:KAUST En organisk halvlederfotokatalysator, der markant forbedrer generering -
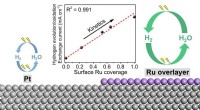 Nye mekanismer for aktivitetsforbedring på bimetalliske katalysatorer til brintproduktion og brænd…Rutheniumatomer understøttet på platin er ekstremt aktive til at producere brint. Kredit:HKUST En gruppe forskere ved Hong Kong University of Science and Technology (HKUST) og Xiamen University ha
Nye mekanismer for aktivitetsforbedring på bimetalliske katalysatorer til brintproduktion og brænd…Rutheniumatomer understøttet på platin er ekstremt aktive til at producere brint. Kredit:HKUST En gruppe forskere ved Hong Kong University of Science and Technology (HKUST) og Xiamen University ha -
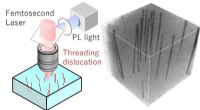 Ikke -destruktiv karakteriseringsteknik hjælper udviklingen af galliumnitridkrystalFig. 1. Målesystem og observationsbillede af TDer i GaN -halvleder ved fotoluminescensmetode med multiphoton -excitation. TDer observeres som mørke linjer. Kredit:Osaka University Fig. 1. Målesystem o
Ikke -destruktiv karakteriseringsteknik hjælper udviklingen af galliumnitridkrystalFig. 1. Målesystem og observationsbillede af TDer i GaN -halvleder ved fotoluminescensmetode med multiphoton -excitation. TDer observeres som mørke linjer. Kredit:Osaka University Fig. 1. Målesystem o
- Giv en operationel definition af acceleration?
- Uddybende spørgsmål:Hvad er et supersolid?
- Sådan finder du prøvestandardafvigelse
- Gasrørsarbejdere finder 800 år gamle lig i Peru
- Rejsegiganten Expedia sender CEO-pakning efter svage resultater
- Fald i atmosfærisk CO2 forårsagede afkøling i dinosaurernes tidsalder


