Hvorfor kulstof danner så mange forbindelser:kraften ved kovalente bindinger
Her er hvorfor det er så vigtigt:
* Kovalente bindinger: Kulstof deler elektroner med andre atomer for at danne stærke kovalente bindinger. Dette gør det muligt for kulstof at binde sig til en lang række elementer, herunder brint, oxygen, nitrogen og andre kulstoffer.
* Fire obligationer: Kulstof har fire valenselektroner, hvilket betyder, at det kan danne fire kovalente bindinger. Dette tillader kulstof at forbinde med flere andre atomer, hvilket skaber komplekse og forskelligartede strukturer.
* Kædedannelse: Kulstofatomer kan binde sig til hinanden i lange kæder og danner rygraden i mange organiske molekyler. Disse kæder kan være lige, forgrenede eller endda cykliske (dannende ringe).
* Dobbelt- og tredobbeltbindinger: Kulstof kan også danne dobbelt- og tredobbeltbindinger med andre atomer, hvilket tilføjer yderligere kompleksitet og variation til dets forbindelser.
Denne evne til at danne flere bindinger med sig selv og andre elementer giver kulstof en bemærkelsesværdig alsidighed, hvilket fører til det store udvalg af organiske forbindelser, vi ser i den naturlige verden og i laboratoriet.
 Varme artikler
Varme artikler
-
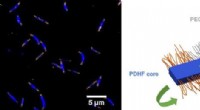 Polymer krystaller er nøglen til rekordstor energitransportBillede, der viser lysemission fra de polymere nanostrukturer og skematisk af en enkelt nanostruktur. Kredit:University of Bristol Forskere fra universiteterne i Bristol og Cambridge har fundet en
Polymer krystaller er nøglen til rekordstor energitransportBillede, der viser lysemission fra de polymere nanostrukturer og skematisk af en enkelt nanostruktur. Kredit:University of Bristol Forskere fra universiteterne i Bristol og Cambridge har fundet en -
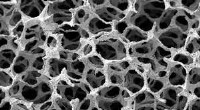 Metallisk skum kan opsuge lyd under højt tryk, miljøer med høje temperaturer såsom jetmotorerEt scanningselektronmikrofotografi af det nikkelbaserede superlegering med åbne celler. Kredit:Singapore Institute of Manufacturing Technology Superlegeringsskum kunne gøre skibs- og flymotorer me
Metallisk skum kan opsuge lyd under højt tryk, miljøer med høje temperaturer såsom jetmotorerEt scanningselektronmikrofotografi af det nikkelbaserede superlegering med åbne celler. Kredit:Singapore Institute of Manufacturing Technology Superlegeringsskum kunne gøre skibs- og flymotorer me -
 Forskere kaster lys over nyt billigt materiale til at se i mørketDr. Wendy Sarney bruger den molekylære stråleepitaximaskine ved US Army Research Laboratory til at producere infrarøde detektormaterialer med en ny synteseproces. Kredit:US Army Forskere ved U.S.
Forskere kaster lys over nyt billigt materiale til at se i mørketDr. Wendy Sarney bruger den molekylære stråleepitaximaskine ved US Army Research Laboratory til at producere infrarøde detektormaterialer med en ny synteseproces. Kredit:US Army Forskere ved U.S. -
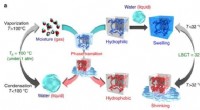 Forskere rapporterer om en temperaturfølsom gel, der absorberer og frigiver fugtIllustration af hovedbegreberne beskrevet i dette papir. Kredit:Kansai University Takashi Miyata ved Kansai University og kolleger melder ind Naturkommunikation en temperaturfølsom gel, der abso
Forskere rapporterer om en temperaturfølsom gel, der absorberer og frigiver fugtIllustration af hovedbegreberne beskrevet i dette papir. Kredit:Kansai University Takashi Miyata ved Kansai University og kolleger melder ind Naturkommunikation en temperaturfølsom gel, der abso
- Materialet, der skjuler supermassive sorte huller
- Hvad er de 5 karakteristiske egenskaber ved stof?
- Hvad er de syv egenskaber ved den lineære korrelationskoefficient?
- Samarbejde:NASAs netværk styrker Artemis I
- Hvad var Alfred Wegeners hypotese om kontinental drift?
- Hvad er forskellene mellem evolutionsteori og modstridende teorier?


