Hydrogens ioniske forbindelser:Gruppe 1 &2 forklaret
1. Alkalimetaller (gruppe 1): Disse metaller, som lithium (Li), natrium (Na) og kalium (K), har en stærk tendens til at miste en elektron for at danne en +1 kation. Hydrogen, i nærvær af disse metaller, får en elektron til at danne en -1 anion (hydridion, H⁻). Dette resulterer i ioniske forbindelser som lithiumhydrid (LiH), natriumhydrid (NaH) og kaliumhydrid (KH).
2. Alkaliske jordmetaller (Gruppe 2): Disse metaller, som beryllium (Be), magnesium (Mg) og calcium (Ca), mister to elektroner og danner +2 kationer. Hydrogen vinder igen en elektron for at danne en hydridion (H⁻), og der kræves to hydridioner for at balancere +2-ladningen af jordalkalimetalet. Eksempler inkluderer berylliumhydrid (BeH2 ), magnesiumhydrid (MgH2 ) og calciumhydrid (CaH2 ).
Sidste artikelNatriumkarbonatkrystallisationsvand:Forståelse af hydrater
Næste artikelGuld:At forstå sin plads i uorganisk kemi
 Varme artikler
Varme artikler
-
 Bøjning af DNA koster mindre energi end antagetKredit:Leiden Institut for Fysik Måden DNA folder i høj grad bestemmer, hvilke gener der udlæses. John van Noort og hans gruppe har kvantificeret, hvor let sammenrullede DNA-dele stables. Dette ko
Bøjning af DNA koster mindre energi end antagetKredit:Leiden Institut for Fysik Måden DNA folder i høj grad bestemmer, hvilke gener der udlæses. John van Noort og hans gruppe har kvantificeret, hvor let sammenrullede DNA-dele stables. Dette ko -
 Hvad er sjældne jordarters grundstoffer? Fire spørgsmål besvaretEn håndfuld europium. Kredit:Alchemist-hp, CC BY-SA De fleste amerikanere bruger sjældne jordarters grundstoffer hver dag – uden at vide det, eller ved noget om, hvad de laver. Det kan ændre sig,
Hvad er sjældne jordarters grundstoffer? Fire spørgsmål besvaretEn håndfuld europium. Kredit:Alchemist-hp, CC BY-SA De fleste amerikanere bruger sjældne jordarters grundstoffer hver dag – uden at vide det, eller ved noget om, hvad de laver. Det kan ændre sig, -
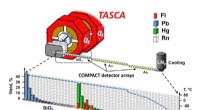 Undersøgelse viser, at flerovium er det mest flygtige metal i det periodiske systemSkematisk visning af eksperimentopsætning. Kredit:A. Yakushev, GSI/FAIR Et internationalt forskerhold fik ny indsigt i de kemiske egenskaber af det supertunge grundstof flerovium - grundstof 114 -
Undersøgelse viser, at flerovium er det mest flygtige metal i det periodiske systemSkematisk visning af eksperimentopsætning. Kredit:A. Yakushev, GSI/FAIR Et internationalt forskerhold fik ny indsigt i de kemiske egenskaber af det supertunge grundstof flerovium - grundstof 114 - -
 Forskere kaster nyt lys over mysterier bag lysudsendelsen fra ildfluerEn hunbille glødende grøn-gult lys. Kredit:NYU Abu Dhabi Et team af forskere fra NYU Abu Dhabis (NYUAD) Smart Materials Lab (SML) ledet af professor i kemi Panče Naumov har gennemført en grundig g
Forskere kaster nyt lys over mysterier bag lysudsendelsen fra ildfluerEn hunbille glødende grøn-gult lys. Kredit:NYU Abu Dhabi Et team af forskere fra NYU Abu Dhabis (NYUAD) Smart Materials Lab (SML) ledet af professor i kemi Panče Naumov har gennemført en grundig g
- Googles Duplex skal have en advarsel, siger ekspert i kunstig intelligens
- Er du, at fysik nogensinde vil være komplet i den forstand, der ikke længere har behov for teoreti…
- Hvad kaldes en horisont også?
- Manuskripter og kunst understøtter beviser på, at syfilis var i Europa længe før opdagelsesrejse…
- Undersøgelse af, hvordan sollys nedbryder plastik på havets overflade
- Forskere, der bruger pulsarmålinger til at undersøge mørkt stof, finder ud af, at Mælkevejsgalak…


