Klorreaktioner:Observerer farveændringer med bromid- og jodidioner
Klors reaktion med bromidioner
* Reaktion: Klor (Cl₂) er et stærkere oxidationsmiddel end brom (Br₂). Når klor reagerer med bromidioner (Br⁻), oxiderer det bromidionerne til brom.
* Farveændring: Opløsningen bliver fra farveløs (bromidioner) til orangebrun (brom).
* Ligning: Cl2(aq) + 2Br-(aq) → 2Cl-(aq) + Br2(aq)
Klors reaktion med jodidioner
* Reaktion: Klor (Cl₂) er et stærkere oxidationsmiddel end jod (I₂). Når klor reagerer med iodidioner (I⁻), oxiderer det jodidionerne til jod.
* Farveændring: Opløsningen bliver fra farveløs (iodid-ioner) til brun-rød (jod).
* Ligning: Cl2(aq) + 2I⁻(aq) → 2Cl⁻(aq) + I₂(aq)
Nøglepunkt: Disse reaktioner viser halogenernes relative styrker som oxidationsmidler. Klor er den stærkeste, efterfulgt af brom og derefter jod.
 Varme artikler
Varme artikler
-
 Undersøgelse af opvarmede tobaksprodukterKredit:Pixabay/CC0 Public Domain En ny artikel, der undersøger, om opvarmede tobaksprodukter udsender røg, er blevet offentliggjort i det akademiske tidsskrift American Chemical Society Omega . Pr
Undersøgelse af opvarmede tobaksprodukterKredit:Pixabay/CC0 Public Domain En ny artikel, der undersøger, om opvarmede tobaksprodukter udsender røg, er blevet offentliggjort i det akademiske tidsskrift American Chemical Society Omega . Pr -
 Team udvikler en familie af bioinspirerede kunstige træsorter fra traditionelle harpikserDet illustrerer, hvordan kunstige træsorter dannes i molekylær skala og detaljer. Kredit:YU Shuhong Naturen har givet inspirationen til design og fremstilling af højtydende biomimetiske ingeniørma
Team udvikler en familie af bioinspirerede kunstige træsorter fra traditionelle harpikserDet illustrerer, hvordan kunstige træsorter dannes i molekylær skala og detaljer. Kredit:YU Shuhong Naturen har givet inspirationen til design og fremstilling af højtydende biomimetiske ingeniørma -
 Blod fra stofbrugere kan afsløre stoffets oprindelseMirjam de Bruin-Hoegée udfører en kemisk analyse med LC-Orbitrap-MS. Kredit:University of Amsterdam Opioiden fentanyl bruges ikke kun i medicinsk praksis som smertestillende, men er også et populæ
Blod fra stofbrugere kan afsløre stoffets oprindelseMirjam de Bruin-Hoegée udfører en kemisk analyse med LC-Orbitrap-MS. Kredit:University of Amsterdam Opioiden fentanyl bruges ikke kun i medicinsk praksis som smertestillende, men er også et populæ -
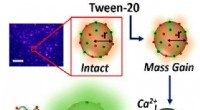 Forskere afslører, hvordan vaskemidler faktisk virkerGrafisk abstrakt. Kredit:The Journal of Physical Chemistry Letters (2022). DOI:10.1021/acs.jpclett.2c00704 Forskere har opdaget den præcise måde, hvorpå rengøringsmidler bryder biologiske membraner
Forskere afslører, hvordan vaskemidler faktisk virkerGrafisk abstrakt. Kredit:The Journal of Physical Chemistry Letters (2022). DOI:10.1021/acs.jpclett.2c00704 Forskere har opdaget den præcise måde, hvorpå rengøringsmidler bryder biologiske membraner
- Hvad er en struktur, der leder cellens arbejde?
- Vejsalte og andre menneskelige kilder truer verdens ferskvandsforsyninger
- Hvordan proteinaggregering sker i celler
- Beskriv bevægelsen af et objekt, der har accelertion 0?
- Hvilken af de følgende reaktioner viser, at dannelse NO2 kræver 33,1 kJ mol?
- Hvad er menneskelig struktur?


