Forstå pH-skalaen:syrer, baser og neutralitet
* 0-6: Meget sur (f.eks. batterisyre)
* 7: Neutral (f.eks. rent vand)
* 8-14: Meget alkalisk (f.eks. blegemiddel)
Her er en opdeling:
* Syrer: Opløsninger med en pH-værdi mindre end 7 betragtes som sure. De frigiver hydrogenioner (H+), når de opløses i vand, hvilket gør opløsningen mere sur.
* Baser: Opløsninger med en pH større end 7 betragtes som basiske eller basiske. De frigiver hydroxidioner (OH-), når de opløses i vand, hvilket gør opløsningen mere basisk.
Vigtige punkter:
* Skalaen er logaritmisk: Det betyder, at hver heltalændring i pH repræsenterer en tidoblet ændring i surhedsgrad eller alkalinitet. For eksempel er en opløsning med en pH på 3 ti gange surere end en opløsning med en pH på 4.
* Neutral: En pH på 7 betragtes som neutral, fordi koncentrationen af hydrogenioner og hydroxidioner er lige store.
Her er nogle eksempler på almindelige stoffer og deres omtrentlige pH-værdier:
* Citronsaft: pH 2
* Eddike: pH 3
* Kaffe: pH 5
* Mælk: pH 6,5
* Rent vand: pH 7
* Natron: pH 9
* Ammoniak: pH 11
* Natriumhydroxid (lud): pH 13
pH-skalaen er essentiel på forskellige områder, herunder kemi, biologi og miljøvidenskab, da den hjælper os med at forstå stoffers egenskaber og deres virkninger på levende organismer og miljøet.
 Varme artikler
Varme artikler
-
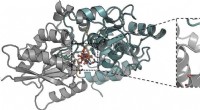 Sultende tuberkulose af sukkerarter kan være en ny måde at bekæmpe det påDetaljer på molekylært niveau af interaktionen af trehalose bundet til den mykobakterielle LpqY-transporter. Kredit:University of Warwick Tuberkulose er en ødelæggende sygdom, der kræver over 1,
Sultende tuberkulose af sukkerarter kan være en ny måde at bekæmpe det påDetaljer på molekylært niveau af interaktionen af trehalose bundet til den mykobakterielle LpqY-transporter. Kredit:University of Warwick Tuberkulose er en ødelæggende sygdom, der kræver over 1, -
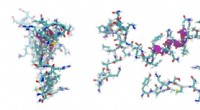 Bioengineer har til formål at forvandle naturens virusbekæmpere til kraftfulde stofferKredit:CC0 Public Domain Blandt de kraftfulde biokemikalier i det menneskelige immunsystem, peptider er en af de bedste. Findes oftest på de steder, hvor mikrober elsker at slå rod - øjets slim
Bioengineer har til formål at forvandle naturens virusbekæmpere til kraftfulde stofferKredit:CC0 Public Domain Blandt de kraftfulde biokemikalier i det menneskelige immunsystem, peptider er en af de bedste. Findes oftest på de steder, hvor mikrober elsker at slå rod - øjets slim -
 Fra medicin til nanoteknologi:Hvordan guld stille og roligt former vores verdenKredit:itti ratanakiranaworn/Shutterstock Det periodiske system med kemiske grundstoffer fylder 150 i år. Jubilæet er en chance for at skinne lys over bestemte elementer - hvoraf nogle virker alle
Fra medicin til nanoteknologi:Hvordan guld stille og roligt former vores verdenKredit:itti ratanakiranaworn/Shutterstock Det periodiske system med kemiske grundstoffer fylder 150 i år. Jubilæet er en chance for at skinne lys over bestemte elementer - hvoraf nogle virker alle -
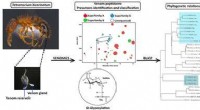 Myrer overgiver deres giftige hemmelighederKredit:American Chemical Society Gifte produceret af snegle, slanger, skorpioner og edderkopper indeholder adskillige bioaktive forbindelser, der kan føre til terapeutiske lægemidler eller insekts
Myrer overgiver deres giftige hemmelighederKredit:American Chemical Society Gifte produceret af snegle, slanger, skorpioner og edderkopper indeholder adskillige bioaktive forbindelser, der kan føre til terapeutiske lægemidler eller insekts
- Blæser et flag i vinden kinetisk af potentiel energi?
- Få den indre historie om produkter med computertomografi
- Hvilken slags klippe dannes ved forvitring og erosion?
- Hvad sker der med kroppen, når kinetisk energi stiger med fire gange?
- Tesla Model 3-ejer implanterer nøglekortchip i hendes arm for at låse op og starte sit køretøj
- Hvad er de fire teorier om, hvor Moon kom fra?


