Kulstof og silicium:Forståelse af 4 valenselektroner til binding
Her er hvorfor:
* Kulstof: Kulstof har et atomnummer på 6, hvilket betyder, at det har 6 elektroner. Dens elektronkonfiguration er 1s²2s²2p². Dette giver den 4 valenselektroner (elektronerne i den yderste skal), som er tilgængelige for binding.
* Silicon: Silicium har et atomnummer på 14 med en elektronkonfiguration på 1s²2s²2p⁶3s²3p². Den har også 4 valenselektroner i sin yderste skal.
Både kulstof og silicium er i gruppe 14 (IVA) i det periodiske system, og de er kendt for deres evne til at danne fire kovalente bindinger på grund af at have fire valenselektroner. Denne egenskab er fundamental for deres rolle i organisk kemi og dannelsen af mange uorganiske forbindelser.
 Varme artikler
Varme artikler
-
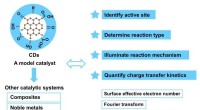 Avancerede multifunktionelle kulstofprikker i fotoelektrokemi-baseret energiomdannelseCarbon dots (CDer) kan bruges som en god modelkatalysator for TPV-testsystemer, og en række forskellige databehandlingsmetoder kan bruges til at opnå dybdegående forskning i det aktive sted, reaktions
Avancerede multifunktionelle kulstofprikker i fotoelektrokemi-baseret energiomdannelseCarbon dots (CDer) kan bruges som en god modelkatalysator for TPV-testsystemer, og en række forskellige databehandlingsmetoder kan bruges til at opnå dybdegående forskning i det aktive sted, reaktions -
 Ny metode til at forbinde præfabrikerede betonbjælker og søjlerAdjunkt Mostafa Tazarv fra Institut for Bygge- og Miljøteknik fører tilsyn med test af en ny metode til at forbinde præfabrikerede betonbjælker og søjler, der gør det muligt at reparere bygninger efte
Ny metode til at forbinde præfabrikerede betonbjælker og søjlerAdjunkt Mostafa Tazarv fra Institut for Bygge- og Miljøteknik fører tilsyn med test af en ny metode til at forbinde præfabrikerede betonbjælker og søjler, der gør det muligt at reparere bygninger efte -
 Smart dug kan finde frugt og hjælpe med at vande planterneDet smarte Capacitivo -stof kan identificere frugt og finde tabte genstande. Samlet set, systemet opnåede en 94,5% nøjagtighed i test. Kredit:Figur med tilladelse fra XDiscovery Lab. Forskere har
Smart dug kan finde frugt og hjælpe med at vande planterneDet smarte Capacitivo -stof kan identificere frugt og finde tabte genstande. Samlet set, systemet opnåede en 94,5% nøjagtighed i test. Kredit:Figur med tilladelse fra XDiscovery Lab. Forskere har -
 In-situ kemiundersøgelser for µSRKredit:Lucy Moorcraft/SINE2020 På grund af den kemiske analogi mellem muonium (et bundet muon-elektronsystem) og brint, muon-teknikken tilbyder en værdifuld metode til at udforske mange mekanismer
In-situ kemiundersøgelser for µSRKredit:Lucy Moorcraft/SINE2020 På grund af den kemiske analogi mellem muonium (et bundet muon-elektronsystem) og brint, muon-teknikken tilbyder en værdifuld metode til at udforske mange mekanismer


